타이타늄 상에 코팅된 클로르헥시딘 항균제를 함유한 수산화인회석의 특성
초록
본 연구에서는 타이타늄 상에 항균제 클로르헥시딘(chlorhexidine; CHX)이 함유된 수산화인회석을 코팅하고 그 특성을 규명하였다. CHX를 혼합한 개조된 생체유사용액(modified simulated body fluid; mSBF)에 타이타늄 디스크를 침적하여 Ti-mSBF-CHX 시편군을 준비하였다. CHX를 함유하지 않은 mSBF에 침적하여 코팅한 Ti-mSBF 시편군을 다시 CHX 용액에 침적하여 Ti-mSBF-adCHX 시편군을 준비하였다. Ti-mSBF 시편 표면에 나노 형태의 결정들로 구성된 구형의 클러스터들이 균일하게 코팅되었다. Ti-mSBF-CHX 시편에서는 이러한 클러스터들과 함께 리본형상의 결정들이 관찰되었으며, 이 결정들에서 높은 CHX 조성이 측정되었다. 두 시편 모두 HAp 결정구조가 지배적이었으며, β-TCP (tricalcium phosphate)와 OCP (octacalcium phosphate) 결정구조가 Ti-mSBF-CHX 시편에서 관찰되었다. FT-IR 스펙트럼은 Ti-mSBF-adCHX와 Ti-mSBF-CHX 시편군에서 CHX의 피크가 강하게 관찰되었다. 그러나 인산완충식염수(phosphate buffered saline;PBS)에 침적한 후, CHX가 Ti-mSBF-CHX 시편에서는 천천히 용출된 반면, Ti-mSBF-adCHX 시편에서는 빠르게 용출되었다. 따라서 Ti-mSBF-CHX 시편은 골과 유사한 HAp 구조를 가지며 함유된 CHX가 지속적으로 방출될 수 있기 때문에 향후 임플란트 시술에서 염증을 방지할 수 있는 코팅법으로 기대된다.
Abstract
In this study, antibacterial chlorhexidine (CHX)-containing hydroxyapatite (HAp) was coated on titanium and investigated its characteristics. Ti-mSBF-CHX group was prepared by soaking titanium disks in the modified simulated body fluid (mSBF) mixed with CHX. Ti-mSBF group was coated using mSBF without CHX. Ti-mSBF-adCHX group was prepared by soaking Ti-mSBF specimen in CHX-containing solution. The crystallines clusters composed with nano-shaped crystallites were coated on the surface of the Ti-mSBF specimen. The ribbon-shaped crystallites were observed with the crystalline clusters on the Ti-mSBF-CHX specimen. The content of CHX chemical compositions was high in ribbon-shaped crystallites. HAp crystalline structure was dominant for all prepared specimens, and β-TCP (tricalcium phosphate) and OCP (octacalcium phosphate) crystalline structures were observed in the Ti-mSBF-CHX specimen. FT-IR spectra showed the strong peaks of CHX in Ti-mSBF-adCHX and Ti-mSBF-CHX groups. However, after immersing in a phosphate buffered saline (PBS), CHX was rapidly released in Ti-mSBF-adCHX group, while it was slowly released in Ti-mSBF-CHX. We expect that the coating method of Ti-mSBF-CHX group could be used for protecting inflammation of titanium implant by incorporating antibacterial agent CHX into HAp layer.
Keywords:
Chlorhexidine, Coprecipitation, Hydroxyapatite, Simulated body fluid, Titanium키워드:
공침법, 생체유사용액, 수산화인회석, 클로르헥시딘, 타이타늄서 론
타이타늄은 정형외과와 치과용 임플란트로서 널리 사용되고 있지만, 임플란트 관련 염증은 합병증을 야기할 수 있다(Oakes 등, 1986; Schmalzried 등, 1992; Garvin 등,1995; Zimmerli 등, 2004). 피부를 통하거나 점막을 통과하는 임플란트인 외부고정핀(external fixation pin)과 치과용 임플란트는 박테리아 감염에 더 취약하다(Green, 1983; Green 등, 1984). 생체친화성인 타이타늄 임플란트는 다양한 박테리아의 생태환경 때문에 생리적 조건하에서 표면에 단백질 층을 형성하는데 이는 감염에 의한 염증 발생에 중요한 요인이 된다. 따라서 임플란트 표면에 유기물이 부착하는 것을 방지하거나 항생물질을 방출하는 표면 코팅 방법들이 연구되어 왔으며, 이것들은 박테리아의 초기 표면 부착을 막는 것으로 보고되고 있다(Lingzhou 등, 2009).
금속 임플란트의 약물전달법은 고분자 또는 세라믹 형태에 약물을 주입하여 표면에 코팅하는 방법들이 적용되었다(Radin 등, 1997; Luke 등, 2003). 또 다른 방법으로는 분자결합(Jose 등, 2005; Edupuganti 등, 2007), 단일층 자가 결합(Mani 등, 2008), 은 나노분자를 임플란트 표면에 끼워 넣는 방법(Cao 등, 2011; Zheng 등, 2012) 들을 통한 임플란트 표면에 약물 자체를 결합시키는 방법들이 보고되었다.
Ca-P 화합물은 생체적합하고 골전도성이 있는 것으로 알려져 있으며 약물 전달체로서도 사용되어 왔다(Kim 등, 2008; Zeng 등, 2009). 항생물질을 다공성의 수산화인회석(hydro-xyapatite; HAp) 안으로 침적시켜 타이타늄 임플란트에 코팅하는 방법도 소개되었다(Engesaeter 등, 2003; Jahoda 등, 2006). 항생제가 함유된 HAp 코팅은 일반적인 HAp 코팅과 비교했을 때, in-vivo 에서 감염 예방을 크게 향상시킬 수 있다(Alt 등, 2006).
타이타늄 임플란트에 HAp를 코팅하는 다양한 물리·화학적인 방법들은 제조과정이 생리환경과는 크게 차이가 있거나 높은 온도로 열처리가 필요하기 때문에 골성장 인자와 같은 생물학적 인자들을 함유시키는 것이 어렵다는 단점이 있다(de Groot, 1987; Freeman, 1992). 타이타늄 금속을 코팅하는 방법 중 공침법(coprecipitation)은 생체유사용액(simulated body fluid; SBF)을 이용하는 방법으로서 SBF에 다양한 생물학적 인자들을 함유시키고 재료들을 침적함으로서 골유사형 아파타이트(bone-like apatite; BLAp)을 코팅하는 방법이다. 이 방법은 생리환경과 유사한 온도와 pH를 갖는 용액에서 코팅이 이루어지기 때문에 함유되는 인자들의 생물학적 특성을 효과적으로 유지시킬 수 있는 장점이 있다(Liu 등, 2001; Luong 등, 2006). 또한 유기물 인자들이 표면에 단순 흡착(adsorption)되면 생체 내에서 빠르게 용출되어 버리는 반면, 공침법을 이용하면 이들이 BLAp의 결정격자에 3차원적으로 화학적 결합하기 때문에 용출이 천천히 이루어지게 된다.
지금까지 소혈청 알부민(bovine serum albumin; BSA)을 모델 단백질로 하는 공침법을 이용한 BLAp 코팅을 통하여 단백질의 함유에 따른 BLAp의 형태, 조성, 결정성의 변화에 대하여 많은 연구가 진행되어 왔다(Wen 등, 1999; Dorozhkin 등, 2003; Feng 등, 2003; Kandori, 2007). Song 등(2012)은 SBF 용액을 제조하는 과정에서 BSA의 혼합 방법을 다르게 한 SBF 용액을 이용하여 고분자 스케폴드로 사용되고 있는 PLGA에 코팅할 때 코팅된 BLAp의 결정구조에 변화가 있다는 것을 보고하였다. 심 등(2016)은 이 방법을 타이타늄에 적용하여 같은 결과를 얻었다.
본 연구에서는 항균제인 클로르헥시딘(chlorhexidine; CHX)을 타이타늄 표면에 적용하고자 한다. CHX는 치태 제거와 치은염 예방에 효과적인 살균제, 치과 영역에서 오랫동안 사용되어온 대표적인 살균제중의 하나이다(Löe, 1970). CHX는 피막 형성을 감소시키고 치아에 대한 세균의 부착기전의 변성, 세균 세포벽의 변성을 일으켜 세포용해를 일으킨다. 또한 여러 구강표면에 친화성이 있어 표면에 흡수된 후 천천히 오랜 시간동안 유효농도로 방출된다(Haskel 등, 1986; Jeffcoat 등, 1998). CHX는 무항생(non-antibiotic) 약물로서 항생제 약물을 사용할 경우 나타나는 내성에 대한 단점을 극복할 수 있다(Lingzhou 등, 2009).
본 연구에서는 공침법을 이용하여 치과 영역에서 광범위하게 사용되고 있는 항균물질인 CHX를 함유한 BLAp 박막을 타이타늄 금속에 코팅하는 방법을 연구하였다. SBF를 제조하는 과정에서 CHX를 혼합하여 공침법으로 타이타늄 표면에 BLAp 박막을 코팅하고, 코팅된 박막의 표면형상, 화학적 조성 및 결정구조를 분석하였다. 또한 코팅된 시편을 인산완충식염수(phosphate buffered saline;PBS)에 다시 침적한 후 CHX 용출 특성을 평가하였다.
재료 및 방법
1. 타이타늄 금속의 전처리
순수한 타이타늄 금속(commercially pure titanium; CP-Ti; ASTM Grade 2) 봉을 직경 20 mm, 두께 1 mm의 디스크 형태로 절단한 후 아세톤으로 기름 성분을 제거(degreasing)하였다. 시편 표면은 SiC 연마지를 사용하여 #240부터 #2000까지 순차적으로 연마한 후, 아세톤, 에탄올과 증류수로 각각 5분간 초음파 세척하였다. 이 시편들을 다시 에탄올로 세척한 후 3차 증류수를 사용하여 최종적으로 세척하고 건조시켰다.
2. 화학적 에칭처리 및 열수처리
단순 가공 처리한 타이타늄 금속 표면은 소수성을 나타내기 때문에 코팅에 어려움이 있기 때문에, 다음과 같은 과정을 통하여 표면처리를 통하여 나노거칠기와 친수성을 부여하였다. 먼저 타이타늄 시편을 5M NaOH 용액에 침적하여 60℃의 항온기 내에서 6시간 동안 보관하여 화학적 에칭처리를 하였다. 에칭 처리된 시편은 즉시 꺼내어 증류수로 세척 후 건조하였다. 이 시편 시편들을 다시 1 L의 0.002 M β-glycerophos-phoric acid disodium salt pentahydrate(β-GP)를 포함하는 pH 11의 알칼리 수용액에 침적시킨 다음 고온멸균처리기(ISA-BC0030-SS, Ilshin autoclave Co., Korea)를 이용하여 180℃에서 6시간 동안 열수처리 하였다.
3. mSBF 용액 제조 및 골유사아파타이트 코팅
BLAp 코팅은 생체유사용액에 제조된 시편들을 침적시키는 방법을 이용하여 수행하였다. 표준 SBF 용액은 사용하여 BLAp를 코팅할 경우 그 코팅 속도가 매우 느리기 때문에 본 연구에서는 칼슘과 인 이온의 농도를 2배로 높인 개조된 생체유사용액 (modified-SBF; mSBF)를 제조하여 사용하였다(심등, 2016).
전처리된 타이타늄 금속 시편 시편을 CHX를 함유하는 mSBF에 바로 침적할 경우 BLAp를 코팅하는 것은 어렵기 때문에, 먼저 mSBF 용액만을 이용하여 시편 상에 BLAp를 코팅하였다. 이를 위하여 타이타늄 금속 시편들을 6 well plate에 각각 침적한 후 mSBF 용액을 10 mL씩 채워서 37℃의 전기로에 보관하였다. SBF 용액을 2일 만에 새 용액으로 교환하였으며, 총 4일 동안 침적시켜 BLAp가 베이스로 코팅된 시편을 제조하였다.
순수한 CHX 분말은 수용액에 용해도가 매우 낮기 때문에 본 연구에서는 chlorhexidine gluconate (Sigma-Aldrich) 용액을 CHX 첨가제로 사용하였다. CHX가 첨가 된 mSBF-CHX 용액은 다음과 같은 과정을 거쳐 제조하였다. 먼저 250 mL의 증류수에 200 μL의 CHX와 0.736 g의 KH2PO4를 희석하고, 이 용액을 최종적으로 500 mL의 mSBF를 만들 때 KH2PO4 대신 사용하여 제조하였다.
이와 같이 제조한 mSBF와 mSBF_CHX 용액에 이미 기저에 BLAp가 코팅된 타이타늄 시편을 침적하여 새롭게 코팅된 시편군을 각각 Ti-mSBF, Ti-mSBF-CHX라고 명명하였다. 또한 공침법을 이용하여 제조한 시편과 비교를 위하여 CHX가 BLAp 상에 단순흡착(adsorption)된 시편은 10 μL의 CHX가 희석된 10 mL의 용액에 Ti-mSBF 타이타늄 시편을 침적한 후 건조하여 Ti-mSBF-adCHX라고 명명하였다.
4. 제조된 시편의 특성 분석
제조된 각 실험군의 표면 미세형상은 주사전자현미경 (scanning electron microscopy; SEM, Hitachi, S-3400N, Japan)을 이용하여 관찰하였다. 또한 화학적 조성 분석은 에너지분산형 X-선 분석기(energy dispersive X-ray spectroscopy; EDS, Horiba, 250, Japan)를 이용하여 수행하였다. 각 시편 코팅막의 결정구조는 X-선 회절분석기 (X-ray diffractometer; XRD; PANalytical, X'Pert PRO, Netherlands)를 이용하여 분석하였다. X-선은 Cu-Kɑ 선(30 mA, 40 kV)을 사용하였으며, 10-90o 범위에서 0.067o/s의 속도로 측정하였다. 표면의 화학적 상태는 푸리에변환 적외선분광분석기(Fourier transformation-infrared spectrophotometer; FT-IR, Perkin Elmer, Spectrum 400, UK)의 ATR (attenuated total reflectance) 악세사리를 이용하여 측정하였다.
또한 CHX 용출 특성을 평가하기 위하여 2 mL의 PBS에 각 시편들을 24 시간 동안 침적하였다. 용출실험 후 각 시편들은 다시 FT-IR 측정을 통하여 CHX의 존재 유무를 확인하였다.
결과 및 고찰
1. 시편의 표면 형상 및 화학적 조성
Fig. 1은 Ti-mSBF와 Ti-mSBF-CHX 시편들의 표면 형상을 관찰한 것이다. Ti-mSBF에서 관찰되는 미세 표면형상은 전형적인 BLAp 형상으로서 수십 마이크로 크기의 클러스터(cluster; 결정송이)들이 균일하게 코팅된 형태를 보여주었다. 확대된 이미지는 이러한 클러스터들은 나노 두께를 갖는 판상형의 결정들의 집합체로 구성되어 있는 것을 보여준다.

SEM images of BLAp layer coated using coprecipitation method for Ti-mSBF (a, c) and Ti-mSBF-CHX (b,d) groups.
CHX가 첨가된 Ti-mSBF-CHX 시편의 경우 Ti-mSBF 시편에 비하여 훨씬 더 큰 수백 마이크로미터에 해당하는 클러스트들이 표면에 분포되어 있다. 또한 리본형의 결정입자들이 클러스터들과 함께 관찰된다. 이와 같이 CHX를 사용한 시편의 표면형상과 미세결정의 형상이 mSBF 만을 사용한 시편과 차이가 있는 것은 mSBF에 함유된 CHX가 BLAp의 결정 성장에 영향을 미쳤다는 것을 알 수 있다.
Table 1은 제조된 시편의 EDS 측정으로부터 구한 각 시편의 화학적 조성을 나타낸 것이다. Ti-mSBF 시편의 경우 Ti 기판에 해당하는 Ti와 HAp 조성에 해당하는 Ca, P, O 만이 확인되었다. Ti-mSBF-CHX 시편에서는 Ti-mSBF 시편과는 다르게 CHX의 성분에 해당하는 C, N, Cl이 관찰되었다. 이 시편에서 기판에 해당하는 Ti 피크가 감지되지 않은 것은 BLAp가 기판 상에 두껍게 코팅되었기 때문이다.
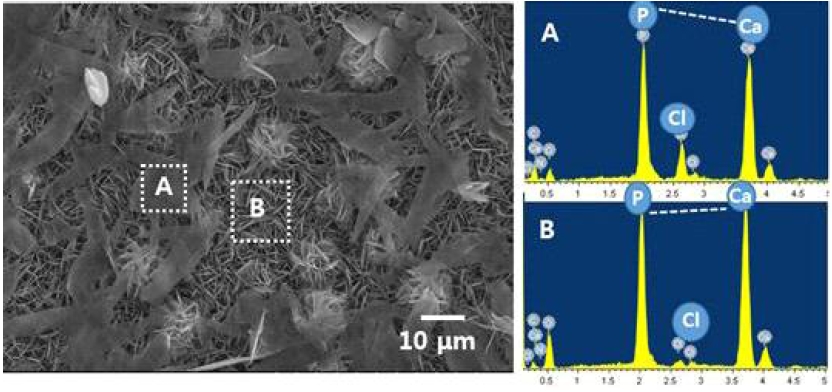
Fig. 2는 Ti-mSBF-CHX 시편에서 관찰된 리본형태의 결정의 조성을 분석하기 위하여 측정한 결과이다. 그림에서 영역 A는 리본이 존재하는 영역이며 영역 B는 순수하게 BLAp 나노 입자만이 존재하는 영역이다. 각 영역에 대한 EDS 스펙트럼을 살펴보면 모두 Ca와 P가 지배적으로 나타나고 있다. 그러나 A 영역에서 Cl의 조성이 B 영역에서 보다 훨씬 더 높게 나타나고 있다. Cl은 CHX에서 유래된 것이므로 리본 결정에 더 많은 양의 CHX가 함유되어 있다는 것을 보여준다. 또한 Fi. 2의 EDS 스펙트럼에서 볼 수 있듯이 A 영역에서의 P 조성에 대한 Ca 조성의 비가 B 영역에서 보다 상대적으로 더 낮았다. 따라서 리본 형태의 결정은 결정구조나 화학적 특성이 전형적인 BLAp 결정들과는 차이가 있을 것으로 예측된다.
2. 시편의 결정구조
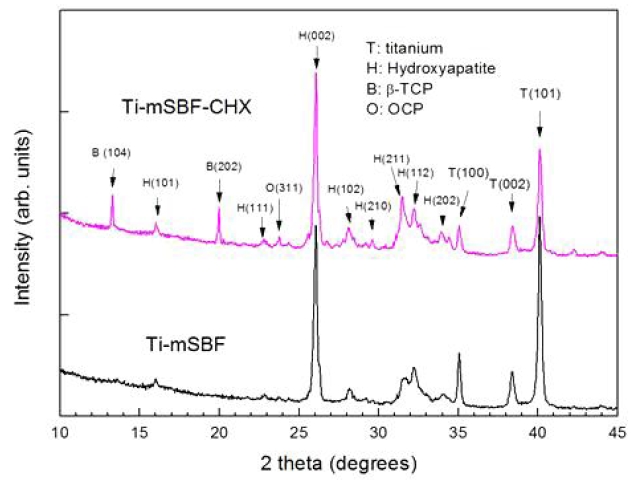
Fig. 3는 각 시편들의 XRD 회절 패턴을 나타낸 것이다. 모든 시편에서 기저금속에 해당하는 Ti 금속 피크가 35o, 38o, 45o에서 관찰되고 있다. 시편에서 가장 강하게 관찰되고 있는 26o 부근의 피크는 HAp 구조의 (002)면에 해당하는 피크로서, 시편 상에 코팅된 물질의 지배적인 구조가 HAp 구조이며, 이 결정들이 c-축 방향으로 더 정렬되어 있다는 것을 알 수 있다. Ti-mSBF-CHX 시편의 경우 Ti-mSBF 시편과는 다르게 13o와 20o에서 β-three calcium phosphate (β-TCP)에 해당하는 피크들이 관찰되고 있다. 또한 octa-calcuim phosphate (OCP) 구조가 해당하는 피크가 23.8o 부근에서 관찰되었다. Ti-mSBF에서와 다르게 나타난 이 피크들은 CHX의 함유와 관련이 있는 것으로 해석된다.
β-TCP와 HAp의 Ca/P 비율 값은 각각 1.5와 1.67로 β-TCP가 HAp에 비하여 상대적으로 Ca 조성이 비율이 낮다. Fig. 2의 EDS 결과는 A 영역의 리본형태의 결정의 Ca/P 값이 B 영역의 BLAp 결정의 값보다 더 작은 것을 보여주었다. 따라서 XRD 피크에서 확인된 β-TCP 결정구조는 이 리본형의 결정에 주로 분포하고 있는 것으로 생각된다.
인산칼슘계 화합물인 β-TCP와 OCP는 HAp를 합성하는 과정에서 중간물질로 자주 관찰되는 물질들이다. 순수한 mSBF 용액에서는 주로 HAp 구조의 화합물이 최종적으로 코팅되지만, mSBF 용액에 CHX가 함유될 경우 CHX의 화학적 작용기들이 무기 이온들과 선택적으로 결합되면서 mSBF에서와는 다른 화학적 결합 환경을 만들어 줄 것이다. 따라서 이러한 화학적 환경들이 Ti-mSBF-CHX 시편의 경우 HAp 구조와 함께 β-TCP 또는 OCP 결정구조의 형성에 영향을 준 것으로 해석된다.
생체재료를 SBF에 침적하여 코팅되는 BLAp 결정은 뼈와 유사한 결정구조와 조성을 갖는 것으로 알려져 있다(Liu 등, 2001). 본 연구에서 CHX를 함유시킨 mSBF를 이용하여 제조한 Ti-mSBF-CHX 시편은 Ti-mSBF와 유사하게 나노 구조를 갖는 HAp 결정들이 지배적으로 코팅되어 있는 것을 알 수 있었다 (Fig. 1과 Fig. 3). 비록 이 시편에서 HAp와 함께 β-TCP와 OCP 구조가 일부 관찰되고 있지만, 기본적으로 코팅된 결정들은 모두 골전도성과 관련된 Ca-P 화합물이다. 따라서 Ti-mSBF-CHX 시편은 CHX를 함유하고 있지만 BLAp 구조와 유사한 형상과 HAp 결정구조를 유지하고 있기 때문에, 골전도성을 유지하면서 항균성을 가질 수 있을 것으로 기대된다.
3. 시편의 화학적 특성
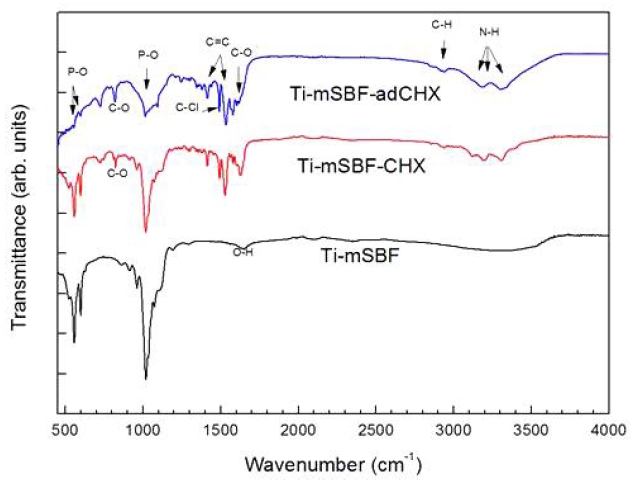
Fig. 4는 각 시편들의 FT-IR 스펙트럼을 나타낸 것이다. mSBF 시편의 경우 전형적인 HAp에 해당하는 FT-IR 스펙트럼으로서 558, 600 및 1019 cm-1에서 관찰된 피크들은 P-O 결합에 해당하는 피크들이다. Ti-mSBF-CHX 시편에서 관찰되는 C=C, C-O, C-Cl, C-H, N-H 피크들은 모두 CHX에 기인한 피크들이다. 따라서 공침법으로 제조한 Ti-mSBF-CHX 시편에 CHX가 잘 함유되어 있는 것을 알 수 있다. 또한 단순하게 CHX 용액을 이용하여 CHX를 표면에 흡착시킨 Ti-mSBF-adCHX 시편의 경우 또한 강한 CHX 피크를 관찰할 수 있었다.
4. 시편의 CHX 용출 특성
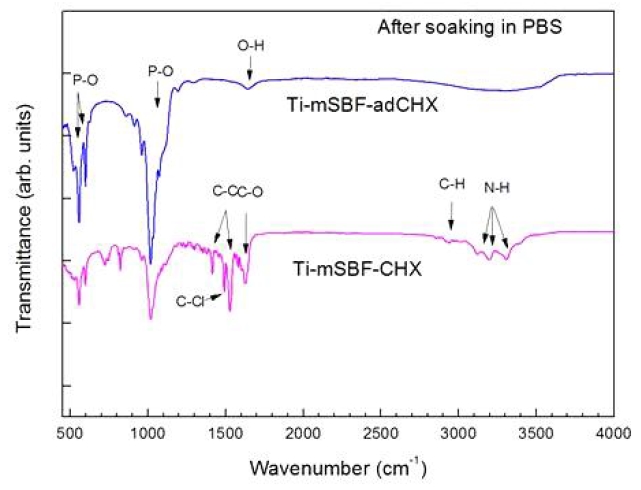
Fig. 5는 각 시편들을 PBS 용액에 24시간동안 침적한 후 이 시편들을 다시 FT-IR로 측정하여 본 결과를 나타낸 것이다. Fig. 6에서 mSBF_adCHX 시편은 CHX가 높은 함량으로 관찰되었지만 24시간 용출 후 CHX 피크들이 모두 사라졌다. 따라서 단순한 흡착에 의하여 HAp 표면에 CHX를 함유시키는 것은 생체에 적용시 너무 빠르게 방출이 일어나서 효율적이지 않을 것이다. 그러나 공침법으로 제조한 Ti-mSBF-CHX 시편의 경우 용출실험 후에도 CHX가 그대로 관찰되고 있는 것을 확인하였다. 이 시편에서는 CHX가 인산칼슘 화합물들과 화학적 결합을 하고 있거나 단순하게 표면에 흡착하고 있는 것이 아니라 3차원적으로 결정 내에 위치하고 있어 시간에 따라 서서히 용출되고 있는 것으로 해석된다. 이렇게 생체 내에서 HAp 결정으로부터 CHX가 천천히 방출되면 장시간에 걸쳐 약물전달 효과를 가지기 때문에 항균제의 효율이 훨씬 더 증대될 것으로 기대된다.
결 론
본 연구에서는 타이타늄 금속 상에 mSBF 용액을 이용한 공침법에 의하여 항균제 CHX가 함유된 BLAp 박막을 코팅하였다. CHX를 함유한 시편(Ti-mSBF-CHX)과 CHX를 함유하지 않은 시편(Ti-mSBF)들의 결정구조는 모두 HAp가 지배적이었으며, 나노 판상형의 결정들로 구성된 결정 클러스터들로 코팅된 표면이 관찰되었다. Ti-mSBF-CHX 시편의 경우 리본형의 결정 형상과 β-TCP와 OCP 결정구조들이 함께 관찰되었다. FT-IR을 분석을 통하여 Ti-mSBF-CHX 시편에 CHX가 함유되어 있는 것을 확인하였다. PBS 용액에 24시간 동안 침적하여 CHX의 용출특성을 평가한 결과, CHX를 단순히 코팅 표면에 흡착 시킨 시편에서는 CHX가 빠른 시간 내에 용출되었지만, 공침법으로 제조한 시편에서는 천천히 용출되었다. 본 연구를 통하여 제조한 Ti-mSBF-CHX 시편은 골과 유사한 HAp 구조를 가지며 함유된 CHX가 지속적으로 방출될 수 있기 때문에 향후 임플란트 시술시 발생할 수 있는 염증을 방지할 수 있는 코팅법으로 기대된다.
Acknowledgments
본 연구는 한국연구재단 일반연구자지원사업(No. 2013-2173)의 지원으로 수행되었음.
References
- 심서윤, 한옥성, 박영준, 송호준, (2016), 타이타늄 상에 코팅된 소혈청 알부민 함유 골유사형 아파타이트의 특성, 대한치과재료학회지, 43(2), p199-206.
-
Alt, V, Bitschnau, A, Osterling, J, Sewing, A, Meyer, C, Kraus, R, Meissner, SA, Wenisch, S, Domann, E, Schnettler, R, (2006), The effects of combined gentamicinhydroxyapatite coating for cementless joint prostheses on the reduction of infection rates in a rabbit infection prophylaxis model, Biomaterials, 27, p4627-4634.
[https://doi.org/10.1016/j.biomaterials.2006.04.035]

-
Cao, H, Liu, X, Meng, F, Chu, PK, (2011), Biological actions of silver nanoparticles embedded in titanium controlled by micro-galvanic effects, Biomaterials, 32, p693-705.
[https://doi.org/10.1016/j.biomaterials.2010.09.066]

-
De Groot, K, Geesink, R, Klein, CP, Seredian, P, (1987), Plasma-sprayed coatings of hydroxylapatite, J Biomed Mater Res, 21, p1375-1381.
[https://doi.org/10.1002/jbm.820211203]

-
Dorozhkin, SV, Dorozhkina, EI, (2003), The influence of bovine serum albumin on the crystallization of calcium phosphates from a revised simulated body fluid, Colloids and Surfaces A: Physicochem Eng Aspects, 215, p191-199.
[https://doi.org/10.1016/s0927-7757(02)00438-7]

-
Edupuganti, OP, Antoci, V Jr, King, SB, Jose, B, Adams, CS, Parvizi, J, Shapiro, IM, Zeiger, AR, Hickok, NJ, Wickstrom, E, (2007), Covalent bonding of vancomycin to Ti6Al4V alloy pins pro-vides long-term inhibition of Staphylococcus aureus coloni-zation, Bioorg Med Chem Lett, 17, p2692-2696.
[https://doi.org/10.1016/j.bmcl.2007.03.005]

- Engesaeter, LB, Lie, SA, Espehaug, B, Furnes, O, Vollset, SE, Havelin, LI, (2003), Antibiotic prophylaxis in total hip arthroplasty: Effects of antibiotic prophylaxis systemically and in bone cement on the revision rate of 22, 170 primary hip replacements followed 0–14 years in the Norwegian Arthroplasty Register, Acta Orthop Scand, 74, p644-651.
-
Feng, B, Chen, J, Zhang, X, (2002), Interaction of calcium and phosphate in apatite coating on titanium with serum albumin, Biomaterials, 23, p2499-2507.
[https://doi.org/10.1016/s0142-9612(01)00384-2]

- Freeman, MAR, (1992), Hydroxyapatite coating of prostheses, J Bone Joint Surg, 74B, p933-934.
-
Garvin, KL, Hanssen, AD, (1995), Infection after total hip arthroplasty. Past, present, and future, J Bone Joint Surg Am, 77, p1576-1588.
[https://doi.org/10.2106/00004623-199510000-00015]

-
Green, SA, Ripley, MJ, (1984), Chronic osteomyelitis in pin tracks, J Bone Joint Surg Am, 66, p1092-1098.
[https://doi.org/10.2106/00004623-198466070-00017]

- Green, SA, (1983), Complications of external skeletal fixation, Clin Orthop Relat Res, 80, p109-116.
-
Haskel, F, Faquenasi, J, Yssim, I, (1986), Effects of subgigical chlorhexidine irrigation in chronic moderate periodontitis, J Periodontol, 57, p305.
[https://doi.org/10.1902/jop.1986.57.5.305]

- Jahoda, D, Nyc, O, Pokorny, D, Landor, I, Sosna, A, (2006), Antibiotic treatment for prevention of infectious complications in joint replacement, Acta Chir Orthop Traumatol Cech, 73, p108-114.
-
Jeffcoat, M, Bray, KS, Ciancio, SG, (1998), Adjunctive use of a subgingical controlled-release chlorhexidine chip reduces probing depth and improves attachment level compared with scaling and root planing alone, J Periodontol, 69, p989.
[https://doi.org/10.1902/jop.1998.69.9.989]

-
Kandori, K, Tsuyama, S, Tanaka, H, Ishikawa, T, (2007), Protein adsorption characteristics of calcium hydroxyapatites modified with pyrophosphoric acids, Colloids and Surfaces B: Biointerfaces, 58, p98-104.
[https://doi.org/10.1016/j.colsurfb.2007.02.014]

-
Kim, WH, Lee, SB, Oh, KT, Moon, SK, Kim, KM, Kim, KN, (2008), The release behavior of CHX from polymercoated titanium surfaces, Surface and Interface Analysis, 40(3-4), p202-204.
[https://doi.org/10.1002/sia.2809]

-
Jose, B, Antoci, V Jr, Zeiger, AR, Wickstrom, E, Hickok, NJ, (2005), Vancomycin covalently bonded to titanium beads kills Staphylococcus aureus, Chem Biol, 12, p1041-1048.
[https://doi.org/10.1016/j.chembiol.2005.06.013]

- Lingzhou, Zhao, Paul, K. Chu, Yumei, Zhang, Zhifen, Wu, (2009), Antibacterial Coatings on Titanium Implants, J Biomed Mater Res Part B: Appl Biomater, 91B, p470-480.
-
Liu, Y, Layrolle, P, Bruijn, JD, Blitterswijk, CV, Groot, KD, (2001), Biomimetic coprecipitation of calcium phosphate and bovine serum albumin on titanium alloy, J Biomed Mater Res, 57, p327-335.
[https://doi.org/10.1002/1097-4636(20011205)57:3<327::aid-jbm1175>3.0.co;2-j]

- Löe, Harald, and C. Rindom, Schiøtt, (1970), The effect of mouthrinses and topical application of chlorhexidine on the development of dental plaque and gingivitis in man, Journal of Periodontal Research, 5.2, p79-83.
-
Lucke, M, Schmidmaier, G, Sadoni, S, Wildemann, B, SchillerR, Haas, NP, Raschke, M, (2003), Gentamicin coating of metallicimplants reduces implant-related osteomyelitis in rats, Bone, 32, p521-531.
[https://doi.org/10.1016/s8756-3282(03)00050-4]

-
Luong, LN, Hong, SI, Patel, RJ, Outslay, ME, Kohn, DH, (2006), Spatial control of protein within biomimetically nucleated mineral, Biomaterials, 27, p1175-1186.
[https://doi.org/10.1016/j.biomaterials.2005.07.043]

-
Mani, G, Johnson, DM, Marton, D, Feldman, MD, Patel, D, Ayon, AA, Agrawal, CM, (2008), Drug delivery from gold and titanium surfaces using self-assembled monolayers, Biomaterials, 29, p4561-4573.
[https://doi.org/10.1016/j.biomaterials.2008.08.014]

- Oakes, JA, Wood, AJJ, (1986), Infections in surgery, N Engl J Med, 315, p1129-1138.
-
Radin, S, Campbell, JT, Ducheyne, P, Cuckler, JM, (1997), Calciumphosphate ceramic coatings as carriers of vancomycin, Biomaterials, 18, p777-782.
[https://doi.org/10.1016/s0142-9612(96)00190-1]

- Schmalzried, TP, Amstutz, HC, Au, MK, Dorey, FJ, (1992), Etiology of deep sepsis in total hip arthrosplasty. The significance of hematogenous and recurrent infections, Clin Orthop Relat Res, 280, p200-207.
-
Song, HJ, Park, YJ, Moon, WJ, Luong, NL, David, HK, (2012), Effects of protein-simulated body fluid mixing methods on characteristics of bone-like mineral, Materials Science and Engineering C, 32, p2501-2507.
[https://doi.org/10.1016/j.msec.2012.07.032]

-
Wen, HB, Wijn, JRD, Blitterswijk, CAV, Groot, KD, (1999), Incorporation of bovine serum albumin in calcium phosphate coating on titanium, J Biomed Mater Res, 46, p245-252.
[https://doi.org/10.1002/(sici)1097-4636(199908)46:2<245::aid-jbm14>3.0.co;2-a]

-
Zeng, P, Zhang, G, Rao, A, Bowles, W, Wiedmann, TS, (2009), Concentration dependent aggregation properties of chlorhexidine salts, International Journal of Pharmaceutics, 367(1), p73-78.
[https://doi.org/10.1016/j.ijpharm.2008.09.031]

- Zheng, Y, Li, J, Liu, X, Sun, J, (2012), Antimicrobial and osteogenic effect of Ag-implanted titanium with a nanostructured surface, Int J Nanomedicine, 7, p875-884.
- Zimmerli, W, Trampuz, A, Ochsner, PE, (2004), Prostheticjoint infections, N Engl J Med, 351, p1645-1654.