
하이드록시아파타이트 디스크에 적용한 항균물질의 Streptococcus mutans에 대한 항균 지속성
초록
하이드록시아파타이트 디스크에 적용한 항균물질들의 항균성이 얼마나 오래 지속되는지 평가하고자 Streptococcus mutans (S. mutans)의 억제에 효과적인 항균물질들을 실험용 불소바니쉬에 혼합하여 각각 1 mM의 농도로 직경 4.8 mm 하이드록시아파타이트 디스크에 5 μL씩 도포하였다. 양성대조군은 10 μg/mL ampicillin, vehicle 대조군은 dimethyl sulfoxide (DMSO)를 불소바니쉬에 혼합하여 적용하였다. 이 디스크를 증류수에 담가 37℃ 진동수조에서 120 rpm의 속도로 30분, 4시간, 1일, 5일, 20일, 30일간 보관 후 한천배지확산시험으로 억제대를 측정하여 항균성을 평가하였다. 모든 항균물질들은 30일까지 항균효과가 지속되었으며, 그 중 Bakuchiol, Bavachromene, Bavachalcone의 항균효과가 30일까지 높게 지속되었다. 항균물질을 불소바니쉬에 첨가함으로써 S. mutans에 대한 항균성과 항균의 지속성을 높일 수 있어 치아우식예방에 유용하게 사용될 수 있을 것으로 사료된다.
Abstract
This study aimed to evaluate the antibacterial activities sustainability of antibacterial agents mixed with experimental fluoride varnish on hydroxyapatite disc against Streptococcus mutans (S. mutans). On the hydroxyapatite disc with 4.8 mm of diameter, 5 μL of 1 mM antibacterial agents mixed with experimental fluoride varnish were applied. Positive control and vehicle control were 10 μg/mL ampicillin and dimethyl sulfoxide (DMSO) mixed with fluoride varnish, respectively. The discs were stored in distilled water in a 37℃ shaking water bath at 120 rpm for 30 minutes, 4 hours, 1 day, 5 days, 20 days, and 30 days. Antibacterial activities were evaluated with the inhibition zone by the agar diffusion test. The antibacterial activities of all antibacterial agents were sustained for 30 days. Among them, Bakuchiol, Bavachromene, and Bavachalcone showed higher antibacterial activities for up to 30 days. The antibacterial agents when mixed in the experimental fluoride varnish with increased and prolonged antibacterial activities can be applied to prevent dental caries effectively.
Keywords:
Sustained antibacterial effect, Fluoride varnish, Antibacterial agents, Streptococcus mutans키워드:
항균 지속성, 불소바니쉬, 항균물질, Streptococcus mutans서 론
Streptococcus mutans (S. mutans)는 치아우식의 주 원인균으로 알려져 있다. 이 균은 당을 분해하여 탈회과정과 재광화 과정을 반복하여 치아우식을 일으키는 것으로 알려져 있다(1). 치아우식을 예방하기 위한 방법에는 여러 가지가 있다. 청결한 구강위생을 위한 잇솔질 방법과, 주기적인 치과의원 및 병원 방문과 치면열구전색, 수돗물 불소농도조절사업, 불소 함유한 치약과 세정제 구강 겔 사용 불소바니쉬 도포 등이 있다(2-6). 불소바니쉬는 불소를 포함한 치아우식 예방 물질 중 가장 효과적인 물질로 알려져 있다(7). 이전 연구에서는 불소바니쉬가 치아우식 예방에 미치는 효과가 74%, APF Gel은 37%, NaF sol은 28%로 보고되었으며 또한 임상적으로 안전하다고 증명되었다(8). 불소바니쉬는 로진과 NaF로 구성되어 치아표면에 불소막을 형성하여 산성물질로부터 치아를 보호한다(9). 불소바니쉬는 치아표면에 도포가 쉽고 나쁜 맛을 가지지 않으며 독성이 없고 또한 도포 시간이 짧아 영·유아에게도 쉽게 처치가 가능하며 과민반응도 낮다고 알려져 있다(10). 구강내에는 다양한 미생물이 존재하며 이러한 미생물로 인한 구강질환을 예방하기 위해 항생제를 이용한다. 항생제는 장기간 사용시 내성균의 출현 및 다양한 부작용을 야기한다(11). 이로 인해 항생 물질을 대신할 천연물 대한 중요성이 높아져 천연물에 대한 연구가 활발하게 이루어지고 있다. 현재까지 구강미생물의 억제에 효과적이라고 보고된 천연 항균물질은 Xanthorrizol [XAN]과 Bakuchiol 정도밖에 없었다(12, 13). Son 등의 연구에서는 Psoralea corylifolia에 들어있는 화학성분 중 Bakuchiol [BAK], Bavachalcone [BCC], Isobavachromene [IBC]과 Bavachromene [BCM] 물질이 S. mutans를 효과적으로 저해하는 것을 알 수 있었다(14). 현재까지는 1990년대에 실험되었던 Propolis와 chlorhexidine에 불소바니쉬를 혼합 연구 사례만 있을 뿐(15), 천연물에 불소바니쉬를 혼합한 연구는 부족한 실정이다. 이전 연구에서는 항균의 지속성을 간단히 평가하기 위하여 polyethylene terephthalate film에 적용하여 실험하였지만(16), 이는 치아 표면과 성분과 성질이 달라 실제 치아에 적용하였을 때와 다른 결과를 보일 수 있다.
이에 본 연구에서는 실제 치아의 법랑질 성분과 비슷한 하이드록시아파타이트 디스크에 항균물질(XAN과 Psoralea corylifolia의 성분인 BAK, BCC, IBC, BCM)을 실험용 불소바니쉬에 혼합하여 도포함으로써 항균성 불소바니쉬의 항균의 지속성을 평가하고자 하였다. 또한 이를 통하여 치아 표면에 적용한 물질의 항균의 지속성 평가방법을 새롭게 수립하고자 하였다.
재료 및 방법
1. 실험용 불소바니쉬 제작
실험용 불소바니쉬의 제작 방법은 Son 등의 연구에서와 같다(14). 간단히 설명하면 45 wt.% 로진, 50 wt.% 에탄올, 5 wt.% NaF로 제작하였다.
2. 항균물질
Xanthorrhizol (XAN; CAS No. 30199-26-9, Santa Cruz Biotechnology, Dallas, TX, USA), Bakuchiol (BAK; CAS No. 10309-37-2, Santa Cruz Biotechnology), Bavachalcone (BCC; CAS No. 28448-85-3, Chemfaces, Hubei, China), Isobavachromene (IBC; CAS No. 52801-22-6, Chemfaces), Bavachromene (BCM; CAS No. 41743-38-8, Chemfaces)을 구입하였다(14). 각 항균물질을 2 mM이 되도록 Dimethyl sulfoxide (DMSO, 99%, CAS No. 67-68-5, Duksan Co., Seoul, Korea)로 희석하고, 실험용 불소바니쉬와 1:1로 혼합하여 각 물질들의 최종농도가 1 mM이 되도록 하였다. 양성대조군은 20 μg/mL Ampicillin (AMP, Sigma-Aldrich Co. LTD., St. Louis, MO, USA)을 실험용 불소바니쉬와 dimethyl sulfoxide (DMSO)를 1:1로 혼합하여 최종 농도가 10 μg/mL가 되도록 하였고, vehicle control로는 실험용 불소바니쉬와 DMSO를 1:1로 혼합한 것을 이용하였다. 음성대조군은 직경 4.8 mm의 하이드록시아파타이트(HA) 디스크(3D Biotek, Bridgewater, NJ, USA) 자체를 사용하였다.
3. 항균의 지속성 시험
항균 물질과 실험용 불소바니쉬의 혼합물을 각각 5 μL씩 멸균된 하이드록시아파타이트 디스크 표면에 균일한 두께로 도포한 후 클린벤치 내에서 자외선으로 30분 동안 살균하였다. 2 mL용 E-P tube에 멸균된 증류수를 하이드록시아파타이트 표면적당 0.3 cm2/ml가 되도록 603 μL를 넣었다(17). 하이드록시아파타이트 디스크는 재료를 적용한 면이 위로 가도록 증류수를 넣은 E-P tube에 한 개씩 넣은 후 37℃의 진동수조(shaking water bath, JSSI-100C, JS Research Inc., Gongju, Korea)에서 120 rpm의 속도로 30분, 4시간, 1일, 5일, 20일, 30일 동안 보관하여 실험물질들이 증류수에 용출되도록 하였다(Figure 1).
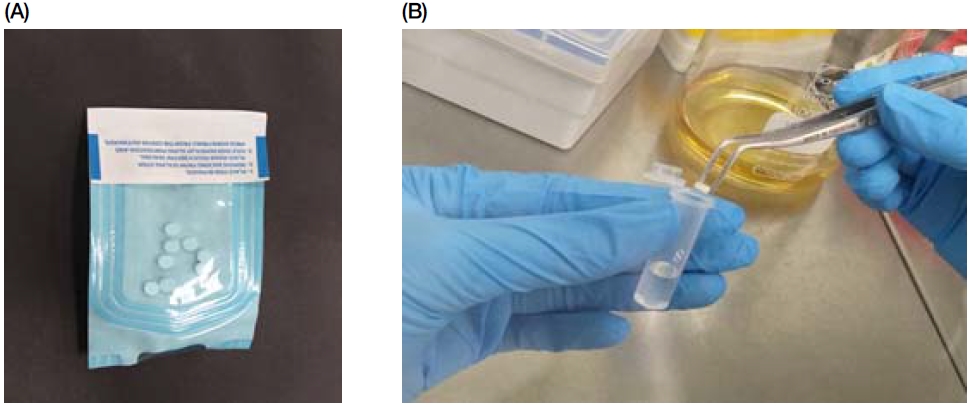
Hydroxyapatite discs sterilized before use (A) and storage of the hydroxyapatite discs applied with the mixture of antibacterial agent and experimental fluoride varnish in distilled water for designated time to evaluate the sustainability of antibacterial activity (B).
치아우식과 관계된 균주인 S. mutans (ATCC 25175)를 brain heart infusion (BHI) 배지에 24시간동안 37℃ CO2 배양기에서 1차 배양 후 200 μL를 다시 BHI 배지에 접종하여 6시간 동안 2차 배양하였다. 세균의 농도가 1.1×109 CFU/mL가 되도록 희석하여 top agar에 균을 혼합한 후 base agar가 깔린 한천배지 위에 접종하였다. 각각의 시간 후 하이드록시아파타이트 디스크를 E-P tube에서 꺼내어 실험물질이 적용된 면이 아래로 향하도록 top agar에 위치시켜 다시 37℃의 CO2 incubator에서 24시간 배양하였다. 하이드록시아파타이트 디스크 주위에 S. mutans의 생장이 억제된 투명 zone의 직경을 직각 방향으로 측정하여 그 평균을 억제대(inhibition zone)로 구하였다(n=16). 각 기간별로 실험물질이 증류수로 용출되고 남은 하이드록시아파타이트 디스크를 이용하여 한천중층배지시험(agar diffusion test)을 실시하여 항균성의 지속성을 평가하였다.
4. 통계분석
통계 분석은 SPSS 프로그램(SPSS 24.0; SPSS GmbH, Munich, Germany)을 이용하였다. 시간에 따른 항균의 지속성 비교와 각 군별로의 항균성을 비교하기 위해 각각 One-way ANOVA를 시행하였고(α=0.05), 사후 검정으로는 Tukey의 다중비교법을 이용하여 사후 검정을 실시하였다.
결 과
항균의 지속성에 대한 결과는 Figure 2에 나타내었고, 사후 검정 결과는 Table 1에 제시되어 있다. 음성대조군인 하이드록시아파타이트 디스크 자체는 억제대가 생기지 않아 아무런 항균효과가 없음이 입증되어 그림과 표에서 제외하였다. 시간이 지남에 따라 억제대의 크기는 감소하였지만, 모든 시험군에서 30일까지 하이드록시아파타이트 디스크의 직경이 4.8 mm 보다 큰 억제대가 형성되어 항균성이 지속되고 있음을 알 수 있었다. 억제대가 형성된 시편의 예를 Figure 3에 나타내었다.
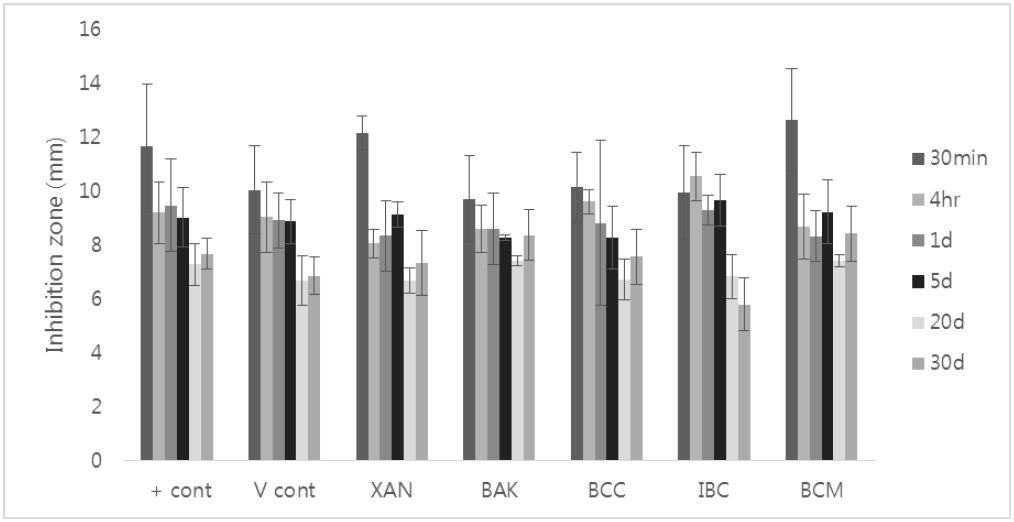
Sustained antibacterial effect of antibacterial agents expressed as inhibition zone against S. mutans measured at 30 minutes, 4 hours, 1 day, 5, 20 and 30 days. + cont: Ampicillin in experimental fluoride varnish. V cont: dimethyl sulfoxide (DMSO) in experimental fluoride varnish.

Sustained antibacterial activities that are expressed as inhibition zones of antibacterial agents incorporated into experimental fluoride varnish against S. mutans on hydroxyapatite discs (unit: mm)
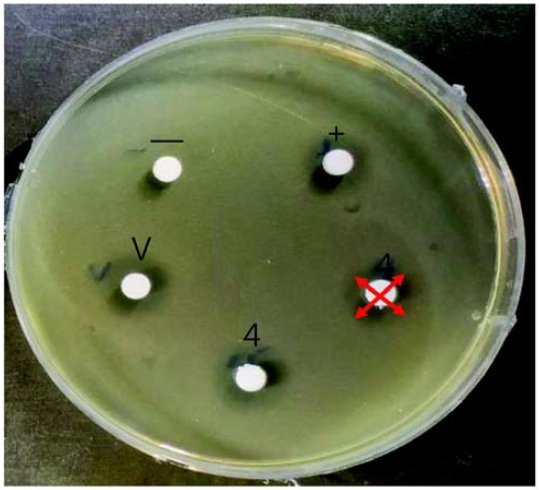
Photograph of the inhibition zone against S. mutans by agar diffusion test formed after cycling in a shaking water bath to evaluate the sustainability of the antibacterial activity. —: negative control that is hydroxyapatite disc (diameter of 4.8 mm) itself, +: positive control that is ampicillin in experimental fluoride varnish (EFV). V: vehicle control: DMSO in EFV. 4: bavachalcone in EFV. The red arrow means the measurement of the diameter of the inhibition zone.
30일에서 Bakuchiol과 Bavachromene의 항균의 지속성 효과가 가장 컸으나(P<0.05), Bavachalcone, Xanthorrhizol 및 양성대조군인 항생제와도 유의성 있는 차이가 없었다(P>0.05).
고 찰
본 연구는 실험용 불소바니쉬를 제작하여 S. mutans의 억제에 효과적인 항균물질들을 혼합하고, 하이드록시아파타이트 디스크에 이 혼합물을 도포하여 이 항균물질들의 항균성이 얼마나 오래 지속되는지 평가하고자 하였다. 항균물질은 Xanthorrhizol과 Psoralea corylifolia에서 추출한 Bakuchiol, Bavachalcone, Isobavacromene, Bavachromene 이용하여 실험을 수행하였다.
실험용 불소바니쉬에 혼합한 모든 군에서 항균성이 30일 동안 지속되어 polyethylene terephthalate film을 사용한 이전 연구에 비해(16), 치아의 법랑질과 비슷한 성분의 하이드록시아파타이트 디스크에 불소바니쉬가 더 효과적으로 오랫동안 부착되어 있다는 것을 알 수 있었다. 본 연구에서 사용한 하이드록시아파타이트 디스크의 성분은 치아의 법랑질 함량 중 무게비로 95%를 차지하기 때문에(18), 치아에 항균물질을 포함한 불소바니쉬를 도포한 경우와 가장 유사한 효과를 얻을 수 있다고 볼 수 있다(19). 따라서 항균의 지속성 시험을 수행하기에는 polyethylene terephthalate film보다는 우치나 표면상태가 일정한 하이드록시아파타이트 디스크가 더 적합하다고 사료된다. 더구나 이전 연구에서는(16), 항균물질들의 농도가 10 mM이었는데 반해, 본 연구에서는 1 mM이었고, 필름의 직경은 5 mm였던 것에 비해 하이드록시아파타이트 디스크의 직경은 4.8 mm였음에도 불구하고 5일 이후의 억제대의 크기가 본 연구에서 상대적으로 넓게 나타났다. 또한 이전 연구에서는 불소바니쉬만 적용한 V cont 군에서 20일부터는 항균성이 나타나지 않았지만(16), 본 연구의 V cont 군에서는 30일까지 항균의 지속성을 보인 점에서 불소바니쉬가 하이드록시아파타이트 표면에 보다 효과적으로 부착됨에 따라 혼합된 항균물질도 더욱 지속적으로 방출할 수 있는 것으로 보인다. Son 등(14)의 연구에 의하면 vehicle control로 사용된 불소바니쉬 자체보다 불소바니쉬와 항균물질을 혼합한 모든 실험군에서 항균효과가 유의성있게 컸기 때문에 항균물질과 불소바니쉬를 혼합하면 상승작용이 나타나는 것으로 보인다.
항균실험결과 30일에서 Bakuchiol과 Bavachromene의 항균의 지속성 효과가 가장 컸으며 심지어 항생제인 양성대조군과 유의한 차이가 없어서 구강미생물 억제용 항생제를 대체할 수 있는 효과적인 천연물질이라 생각된다. 이전 연구에서는 Bavachalcone의 항균의 지속성이 가장 컸는데(16), 본 연구에서는 비록 Bavachalcone과 유의성있는 차이는 없었지만 Bakuchiol과 Bavachromene의 항균의 지속성 효과가 가장 컸다. Psoralea corylifolia 추출물의 항균활성은 그람음성균보다 S. mutans와 같은 그람양성균에서 높은 항균활성을 나타낸다고 보고되며, Psoralea corylifolia 추출물은 낮은 수용성에도 불구하고 hydroxyl group이 있어 항균력은 페놀 화합물의 함량과 연관이 있을 것으로 사료된다(20). Bakuchiol, Bavachromene, Bavachalcone과 Isobavachromene은 화학구조가 비슷하지만 페놀화합물과와 hydroxyl group의 수가 서로 약간 다른데, 이러한 차이는 Bakuchiol, Bavachromene과 Bavachalcone이 Isobavachromene보다 항균의 지속성이 30일에서 더 높은 이유 중의 하나가 될 것이다(14).
Psoralea corylifolia 추출물 중 Bakuchiol의 항균기전만 알려져 있는데, S. mutans가 치아에 접착하는 것을 방해하는 것으로 알려져 있으며, 구강미생물 예방 및 치료에 유용한 화합물로 식품첨가물 및 구강세정제에 사용될 수 있다고 보고되었다(13). 또한 Psoralea corylifolia의 뿌리부분은 치아우식증에 효과적이라고 보고되고 있다(21). Bavachromene과 Bavachalcone은 구강 내 S. mutans 균주 억제에 효과적이라고 보고되고 있다(22). 나머지 다른 물질들의 구강미생물에 대한 항균효과는 알려져 있지 않지만, 페니실린에 내성이 있는 균주를 포함한 Staphylococus citreus, S. aureus, S. albus 등의 균들의 성장을 억제시킨다고 보고되고 있다(21). Xanthorrhizol은 이전 연구에서 식용식물(C. xanthorrhiza Roxb)로부터 추출되어 S. mutans을 제거하고 억제하는 항균제로서의 가능성을 보여주었다(23).
최근 항생제 남용 및 부작용에 대한 문제의 심각성이 대두되고 있어 구강미생물에 대한 항생제의 일시적인 효과보다는 천연물질을 이용한 항균효과에 관심이 높아지고 있으며, 본 연구에서와 같이 불소바니쉬에 혼합하여 치아에 적용하면 치아우식에 지속적인 예방효과를 나타낼 수 있을 것이라 사료된다. 본 연구에서는 S. mutans에 항균성이 있는 천연물질을 불소바니쉬와 혼합하여 하이드록시아파타이트 디스크에 적용함으로써 항균의 지속성을 측정하였으며, 항균의 지속성에 대하여 보다 적절한 시험방법이 수립되었다고 사료된다. 실험용 불소바니쉬와 혼합한 5가지 항균물질 중 Bakuchiol, Bavachromene, Bavachalcone과 Xanthorrhizol은 항생제와 필적한 정도의 항균의 지속성을 보여, 항균성 불소바니쉬로서의 사용가능성이 제시되었다.
결 론
본 연구에서는 S. mutans에 대한 효과적인 항균물질을 실험용 불소바니쉬에 혼합하여 하이드록시아파타이트 디스크에 적용함으로써 항균의 지속성 시험을 실시한 결과 항균의 지속성은 모든 군에서 30일 동안 지속되었다. 30일에서의 항균효과는 Bakuchiol과 Bavachromene이 가장 컸으며, Bavachalcone, Xanthorrhizol및 양성대조군과 유의한 차이가 없었다. 따라서 S. mutans에 대한 항균성 불소바니쉬의 항균의 지속성을 평가하기 위한 적절한 시험 방법이 수립되었으며, 항균물질 중 Bakuchiol, Bavachromene, Bavachalcone과 Xanthorrhizol은 불소바니쉬에 적용하여 치아우식을 예방하기 위한 항균성 불소바니쉬를 개발할 수 있을 것으로 사료된다.
Acknowledgments
이 성과는 2018년도 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(No. 2018R1A2B6002088). The biological resources used in this research were distributed from KCTC (http://kctc.kribb.re.kr).
References
-
Dame-Teixeira N, Deng D, Do T. Streptococcus mutans transcriptome in the presence of sodium fluoride and sucrose. Arch Oral Biol. 2019;102:186-92.
[https://doi.org/10.1016/j.archoralbio.2019.04.020]

-
Kumar S, Tadakamadla J, Johnson NW. Effect of toothbrushing frequency on incidence and increment of dental Caries. J Dent Res. 2016;95(11):1230-6.
[https://doi.org/10.1177/0022034516655315]

-
Papageorgiou SN, Dimitrak, D, Kotsanos N, Bekes K, van Waes H. Performance of pit and fissure sealants according to tooth characteristics. J Dent, 2017;66:8-17.
[https://doi.org/10.1016/j.jdent.2017.08.004]

- Jadav UG, Acharya BS, Velasquez GM, Vance BJ, Tate RH, Quock RL. Sources of drinking water in a pediatric population. Pediatr Dent. 2014;36(7):474-7.
-
Schwendicke F, Stolpe M. In-office application of fluoride gel or varnish: cost-effectiveness and expected value of perfect information analysis. Caries Res. 2017;51(3):231-9.
[https://doi.org/10.1159/000458729]

-
Anderson M, Dahllöf G, Soares FC, Grindefjord M., Impact of biannual treatment with fluoride varnish on tooth-surface-level caries progression in children aged 1-3 years. J Dent. 2017;65:83-8.
[https://doi.org/10.1016/j.jdent.2017.07.009]

-
Beltrán-Aguilar ED, Goldstein JW, Lockwood SA. Fluoride varnishes. A review of their clinical use, cariostatic mechanism, efficacy and safety. J Am Dent Assoc. 2000;131(5):589-96.
[https://doi.org/10.14219/jada.archive.2000.0232]

-
Sar Sancakli H, Austin RS, Al-Saqabi F, Moazzez R, Bartlett D. The influence of varnish and high fluoride on erosion and abrasion in a laboratory investigation. Aust Dent J. 2015;60(1):38-42.
[https://doi.org/10.1111/adj.12271]

-
Dantas EM, Amorim FK, Nóbrega FJ, Dantas PM, Vasconcelos RG, Queiroz LM. Clinical efficacy of fluoride varnish and low-level laser radiation in treating dentin hypersensitivity. Braz Dent J. 2016;27(1):79-82.
[https://doi.org/10.1590/0103-6440201602422]

-
Fani MM, Kohanteb J, Dayaghi M. Inhibitory activity of garlic (Allium sativum) extract on multidrugresistant Streptococcus mutans. J Indian Soc Pedod Prev Dent. 2007;25(4):164-8.
[https://doi.org/10.4103/0970-4388.37011]

- Kwak DJ. Antibacterial activities of phellodendri cortex on the Streptococcus mutans. J Den Hyg Sci. 2004;10(2):99-107.
-
Rukayadi Y, Hwang JK. In vitro activity of xanthorrhizol against Streptococcus mutans biofilms. Lett Appl Microbiol. 2006;42(4):400-4.
[https://doi.org/10.1111/j.1472-765X.2006.01876.x]

-
Katsura H, Tsukiyama RI, Suzuki A, Kobayashi M. In vitro antimicrobial activities of bakuchiol against oral microorganisms. Antimicrob Agents Chemother. 2001;45(11):3009-13.
[https://doi.org/10.1128/AAC.45.11.3009-3013.2001]

-
Son JL, Kim AJ, Oh SH, Bae JM. Inhibitory effects on Streptococcus mutans of antibacterial agents mixed with experimental fluoride varnish. Dent Mater J. 2020;39(4):690-5.
[https://doi.org/10.4012/dmj.2020-016]

-
Bossù M, Saccucci M, Salucci A, Di Giorgio G, Bruni E, Uccelletti D, et al. Enamel remineralization and repair results of biomimetic hydroxyapatite toothpaste on deciduous teeth: an effective option to fluoride toothpaste. J Nanobiotechnology. 2019;17(1):17.
[https://doi.org/10.1186/s12951-019-0454-6]

-
Son JL, Bae JM. Sustainability of the antibacterial activity of experimental fluoride varnish mixed with antibacterial agents against Streptococcus mutans. J Dent Mater. 2020;47(2):63-70.
[https://doi.org/10.14815/kjdm.2020.47.2.63]

- International Organization for Standardization. ISO 10993-12:2012. Biological evaluation of medical devices—Part 12: Sample preparation and reference materials. Geneva: ISO; 2012.
- Kim MY, Kwon HK, Kim BI. The comparison of remineralizing effect on mouthrinse containing nano sized or micro sized hydroxyapatite. J Korean Acad Dent Health. 2006;30(3):325-34.
-
Mazzoni A, Tjäderhane L, Checchi V, Lenarda RD, Salo T, Tay FR, et al. Role of dentin MMPs in caries progression and bond stability. J Dent Res. 2015Feb;94(2):241-51.
[https://doi.org/10.1177/0022034514562833]

-
Garima Kapoor, Saurabh Saigal, Ashok Elongavan. Action and resistance mechanisms of antibiotics: A guide for clinicians. J Anaesthesiol Clin Pharmacol. 2017;33(3):300–5.
[https://doi.org/10.4103/joacp.JOACP_349_15]

-
Khushboo PS, Jadhav VM, Kadam VJ, Sathe NS. Psoralea corylifolia Linn.-“Kushtanashini”. Pharmacogn Rev. 2010;4(7):69-76.
[https://doi.org/10.4103/0973-7847.65331]

-
Son JL, Kim AJ, Oh SH, Bea JM. Minimum inhibitory concentration and minimum bactericidal concentration of antibacterial fluoride varnish. Korean J Dent Mater. 2018;45(2):139-46.
[https://doi.org/10.14815/kjdm.2018.45.2.139]

-
Nakahara K, Kawabata S, Ono H, Ogura K, Tanaka T, Ooshima T, Hamada S: Inhibitory effect of oolong tea polyphenols on glycosyltransferases of mutans Streptococci. Appl Environ Microbiol 1993;59(4):968-73.
[https://doi.org/10.1128/AEM.59.4.968-973.1993]

