수증기 첨가 상온 대기압 플라즈마의 미백 효과
Abstract
The purpose of this study was to evaluate the tooth bleaching effect by the use of nonthermal atmospheric pressure plasma supplied by humid air(humid air plasma) along with 5 %, 15 %, and 35 % of hydrogen peroxide(HP). A total number of 90 stained teeth were divided into 9 groups(n=10) and treated in different bleaching conditions: only HP, HP with air plasma, and HP with humid air plasma. Color changes(ΔE* ) were measured after three consecutive bleaching using spectrophotometer and National Bureau of Standards systems. One-way ANOVA combined with post-hoc test using Tukey’s method was performed for the statistical analysis. The results showed that final ΔE* values increased significantly in all groups(p<0.05), indicating the effective tooth bleaching. The most significant color changes were noted on samples treated with 15 % HP humid air plasma, 35 % HP air plasma and 35 % HP humid air plasma(p<0.05), but there were no significant differences amongst them(p>0.05). This study suggested that tooth treated by HP with humid air plasma is more effective for tooth bleaching compared to only HP and HP with air plasma. Lastly, it is concluded that using 15 % HP in conjunction with humid air plasma is more safe compared to simply using 35 % HP.
Keywords:
Tooth bleaching, Hydrogen peroxide, Nonthermal atmospheric pressure plasma, HumidityⅠ. INTRODUCTION
치아 미백은 변색된 치아의 색조를 개선하는 방법으로써, 심미성에 대한 대중의 관심이 증가함에 따라 보편적인 시술 방법으로 자리 잡았다. 치아 미백의 효과는 미백제의 조성, 농도, 적용 시간, 적용 횟수, 활성 방법 등에 따라서 좌우되며(Joiner, 2006), 보다 간단한 술식으로 생체안전성을 확보하면서도 빠르고 지속적인 미백 효과를 얻기 위해 다양한 연구가 이루어지고 있다.
1884년 Harlan에 의해 최초로 과산화수소수(hydrogen peroxide; HP)를 이용한 미백 효과가 보고되었다. HP의 작용 기전은 명확히 밝혀지지 않았으나, HP로부터 유래된 하이드록실 라디칼(hydroxyl radical)이 치아에 부착된 착색 유기물을 분해시켜 색조를 개선한다는 이론이 가장 널리 받아들여지고 있다(Joiner, 2004; Kawamoto와 Tsujimoto, 2004).
HP의 농도는 주로 5 %에서 35 %의 범위 내에서 사용되어 왔다. HP 5 %는 트레이를 이용하여 환자가 집에서 스스로 미백 처치를 할 수 있는 자가 미백제로, HP 15 % 및 35 %는 전문가 미백제로 사용되었다. 고농도의 HP를 이용할수록 신속하고 강한 미백 효과를 얻을 수 있다(Moraes 등, 2006). 그러나 HP를 사용한 실활치 미백 시 상아세관 내 확산을 통한 치경부 외흡수(external cervical resorption)가 일어날 수 있으며(Heithersay, 1999), 생활치에 적용 시 법랑질의 표면 성질에 영향을 미치거나 주변 조직의 지각과민증을 유발할 수 있다(Haywood, 2002; Naik 등, 2006). 이처럼 고농도 HP의 적용으로 인한 부작용 사례는 지속적으로 보고되고 있으며, 이를 반영하여 식품의약품안전처는 15 % 이하의 미백제 사용을 권고하였다. Leonard 등(1998)에 의하면 저농도의 미백제를 여러 번 적용할 경우 결과적으로 고농도의 미백제와 같은 수준의 결과를 가져온다는 보고가 있었으나, 임상에서는 적은 방문 횟수로 높은 미백 효과를 얻을 수 있는 방법을 선호하는 실정이다.
이로 인해 저농도에서도 다양한 활성 방법을 통해 단시간에 안전하면서도 고농도에 상응하는 효과를 나타내기 위한 시도가 이루어지고 있다. 그중 상온 대기압 플라즈마를 이용하는 방법은 대기압 하에서 저온의 가스 온도로도 화학적으로 활성화된 라디칼을 생성할 수 있는 방법으로써, 작용 거리, 방전 가스 조성, 조사 시간 및 횟수 등을 조절하여 미백 효과를 개선하고자 하였다(Lee 등, 2009). 플라즈마만 단독 조사하여도 미백 효과가 나타나지만 미백제에 플라즈마를 추가 조사했을 경우 더욱 우수한 미백 효과가 일어난다(Tavares 등, 2003). 2015년 Choi는 미백제 없이 산소 혹은 수증기 첨가 시 플라즈마의 미백 효과가 증가함을 보고하였으나, HP의 농도에 따른 플라즈마의 미백 효과에 대해 추가적인 연구가 필요하다.
따라서 본 연구에서는 우전치 법랑질 표면에 5 %, 15 %, 35 % 농도별로 HP를 적용하고, 방전 가스의 수증기 함유량을 조절한 상온 대기압 플라즈마를 추가 조사함으로써 치아 색조 변화에 미치는 영향에 대해 비교하고자 하였다.
Ⅱ. MATERIALS AND METHODS
1. 연구 재료
본 연구에 사용된 치아는 실험 오차를 줄이기 위해 발치 후 3개월 미만의 우전치를 사용하였으며, 초기 L*값(명도 지수)이 평균 80이고 육안으로 관찰했을 때 특정 우식 병소가 없는 치아를 선별하였다. 준비한 우전치는 실험 전까지 thymol (Sigma, St. Louis, MO, USA) 0.1 % 용액에 넣어 –4 ℃ 조건 하에 보관하였다.
2. 연구 방법
총 100개의 우전치를 3 mm × 7 mm × 3 mm의 시편 형태로 자른 후 법랑질이 표면으로 노출되도록 내경 11 mm, 높이 10 mm로 재단된 유리관의 중앙에 넣고 자가중합형 아크릴릭 레진(Polycoat; Aekyung, Chungnam, Korea)에 매몰하여 24시간 동안 경화시켰다. 경화된 시편은 균일한 법랑질 표면을 얻기 위하여 지속적으로 냉각수가 흐르는 자동연마기(ECOMET III Grinder/Polisher, Buehler Ltd, Lake Bluff)에 600, 1200, 2000 grit의 연마지를 이용하여 단계적으로 연마하였다. 연마된 시편은 착색 과정을 위해 0.12 N(1 %) 염산 용액에 60초간 침적시킨 후, 탄산나트륨 과포화 용액에 30초간 침적하고 마지막으로 1 % 피트산 용액에 60초간 침적하였다. 모든 과정이 끝나면 증류수로 세척하였다.
시편의 착색은 Stookey 방법(Stookey 등, 1982)을 채택하였다. 착색 용액은 121 ℃에서 15분간 멸균된 Typticase Soy Broth(TSB; Becton, Sparks, MD, USA) 배지 800 ml에 균일한 입자의 인스턴트 커피 분말 2.7 g, 홍차 분말 2.7 g, gastric mucin 분말 2.0 g 및 0.1 %의 FeCl30.8 g을 넣고 교반하여 완전히 용해시킨 후 –4 ℃ 조건 하에 보관하였다. 이후 인큐베이터에서 24시간 동안 배양한 Micrococcus luteus 배양 용액 26 ml를 첨가하여 착색 용액을 제조하였다. 효과적인 착색을 위해 37 ℃ 조건 하에서 시편의 침적과 건조를 반복하여 총 7일간 착색시켰다. 시편 용액은 4일마다 교체하였으며, 착색 과정이 종료된 후에는 시편 표면에 착색 용액의 잔여물이 남지 않도록 완전히 증류수로 세척한 후 10분간 건조한 뒤 –4 ℃ 조건 하에 보관하였다.
미백제는 치과용 연마제(Brite powder, Pac Dent International Inc., USA) 90 mg에 과산화수소 용액(Hydrogen peroxide, HP; Sigma, St.Louis, MO, USA) 5 %, 15 %, 35 % 1 ml을 각각 첨가하여 균일한 페이스트 형태로 제조한 후 차광 유리병에 보관하였다. 제조한 미백제는 시린지에 담아 치아 시편 상단에 1 mm 두께로 동량 분배한 후 마이크로브러쉬로 균일하게 도포하였다. 이 상태로 상온에서 10분간 미백처치 후 증류수가 담긴 세척병을 이용하여 10초간 미백제를 씻어내고 건조하는 것을 1회로 설정하여 총 3회 반복하였다.
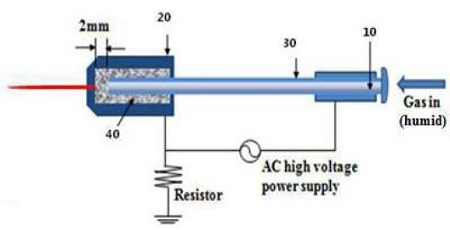
상온 대기압 플라즈마는 광운대학교 플라즈마 바이오과학 연구센터(Plasma Bio-science Research Center, Seoul, Korea)에서 개발한 장비를 사용하였다. 플라즈마 방전용 가스는 유량 1000 sccm의 압축 공기가 증류수 수조를 통과하도록 설계하여 수증기 첨가 비율을 1중량%로 설정하였다. 플라즈마 조사 시 플라즈마 방전 영역이 시편 중앙에 오도록 위치하였으며, 플라즈마 조사구는 미백제가 도포된 법랑질 표면으로부터 3 mm 상단에 고정하였다. 플라즈마를 10분간 조사한 후 증류수가 담긴 세척병을 이용하여 10초간 미백제를 씻어내고 건조하는 것을 1회로 설정하여 총 3회 반복하였다.
착색 시편의 초기 L*값이 60 이하인 90개의 시편을 선정하여 군 당 10개씩 총 9군으로 분류하였다. 각 시편의 L*값은 통계적 유의차가 없음을 확인하였다. 실험군 설정은 Table 1과 같이 5B는 HP 5 %만 10분간 적용하였고, 5BP는 HP 5 %에 상온 대기압 플라즈마를 10분간 조사하였다. 5BPH는 HP 5 %에 수증기를 첨가한 상온 대기압 플라즈마를 10분간 조사하였다. 뒤이어 15B, 15BP, 15BPH는 HP 15 %를, 35B, 35BP, 35BPH는 HP 35 %를 사용하여 5B, 5BP, 5BPH와 동일한 미백 처리 조건 하에서 시행하였다.
미백제의 효과에 대한 색지수 평가는 분광분석계(Spectro photometer, CM-3500d, Minolta, Osaka, Japan)를 이용하여 각 시편 당 3부위에서 L*, a*, b* 값을 측정하여 평균값을 이용하였다. 측정 시점은 착색 후와 1차, 2차, 3차 미백 처리 직후에 각각 측정하였다. 미백 효과에 따른 색조변화량(ΔE*)을 확인하기 위해 ΔL*, Δa*, Δb* 값을 각각 구한 뒤 하단 공식에 의해 도출하였다(Lenhard, 1996).
이 ΔE*값을 하단의 NBS(National Bureau of Standards) 공식으로 변환하여, Table 2와 같이 육안으로 판단 가능한 색조 변화의 정도를 확인하고자 하였다(Shotwell과 Razzoong, 1992).
NBS unit = ΔE* × 0.92
3. 자료 분석
분광분석 측정으로 도출된 색지수 데이터는 통계분석 프로그램인 SPSS(PASW Statistics 20.0, SPSS Inc Co., Chicago, USA)을 이용하여 분석하였다. 각 군당 10회씩 실험하여 평균과 표준편차를 도출하였다. 실험군 간의 변화량의 차이를 확인하기 위해 one-way ANOVA를 실시하였으며, 사후검정은 유의수준 0.05의 Scheffe test를 이용하였다.
Ⅲ. RESULTS AND DISCUSSION
1) 미백 처치 횟수에 따른 치아 미백 효과
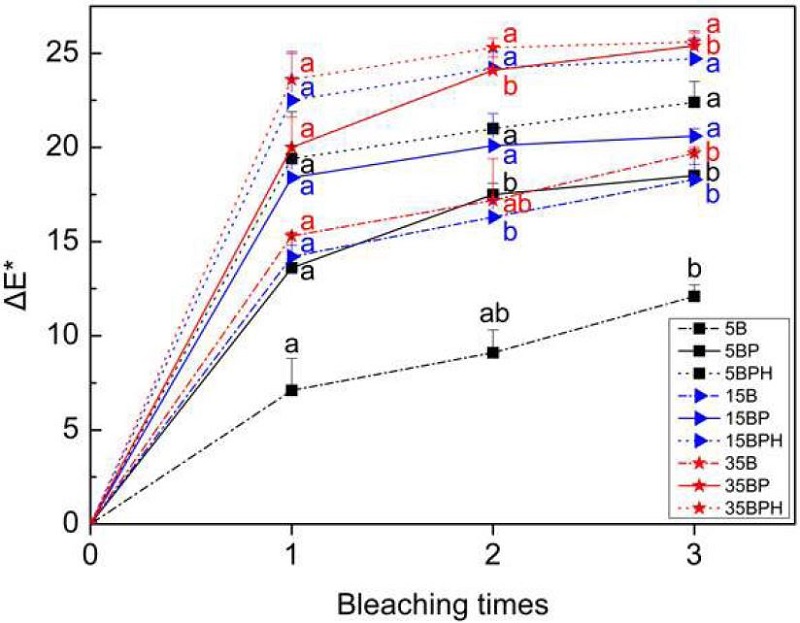
모든 실험군의 1차, 2차, 3차 미백 처치 횟수에 따른 색조 변화량(ΔE*)은 Figure 2에 나타내었으며, 각 9가지 미백 방법의 처치 횟수에 따른 유의차는 각기 다른 영어 소문자로 표시하였다. 1차 미백 처치 후 미백 처리 전에 비해 모든 군에서 ΔE*값이 유의하게 증가하였다(p<0.05). 2차 미백 처치 후 1차에 비해 5BP, 15B, 35BP에서 유의한 ΔE*값의 증가를 보였다(p<0.05). 최종 3차 미백 처치 후 2차에 비해 모든 군에서 ΔE*값이 약간 증가하는 경향을 보였으나 통계적으로 유의한 차이는 없었다(p>0.05). 따라서 3차 처치만으로도 충분한 미백 효과를 얻을 수 있을 것으로 예상되나, 미백 처치 횟수의 증가를 통한 추가 연구가 필요할 것으로 사료된다.
2) 미백 처리 조건에 따른 치아 미백 효과
처리 조건에 따른 치아 미백 효과는 Table 3에 제시하였으며, 동일한 미백제 농도와 미백 횟수에서 플라즈마 조건에 따른 유의차는 영어 소문자로 표기하였다. 5 %의 미백제를 처리하였을 경우 1차, 2차, 3차 모두 단독으로 처리했을 때보다 플라즈마를 적용했을 때 ΔE*값이 유의하게 증가하였다(p<0.05). 또한 일반 공기를 방전 가스로 사용했을 때보다 수증기를 첨가했을 경우에 가장 높은 ΔE*값을 보였다(p<0.05). 이 경향은 15 %의 HP에서도 동일하게 나타나므로, 15 % 이하의 농도에서는 수증기를 함유한 플라즈마를 조사하는 것이 미백 효과를 증진시킴을 알 수 있다. 또한 35 %의 미백제를 1차 처리하였을 때 35B, 35BP, 35BPH 간에는 유의한 차이로 ΔE*값이 증가하였으나(p<0.05), 2회 및 3회 미백 시에는 35BP와 35BPH 간에 유의한 차이를 보이지 않았다(p>0.05). 1차 처리했을 때 수증기 첨가 조건에서 미백 효과가 증진되는 것은 방전 가스에 존재하는 대기 중의 산소를 활성화 시키는 것보다 수증기를 첨가했을 경우 활성 산소의 생성량이 더욱 많아지기 때문이다(Choi 등, 2015). 또한 미백 처리 과정 중 플라즈마의 열 및 가스 흐름으로 인해 미백제의 건조가 일어나는 문제점도 영향을 주었을 것으로 보이며 이를 개선한다면 보다 빠른 시간 내에 우수한 미백효과를 얻을 수 있을 것으로 보인다. 2차부터 35BP와 35BPH간의 차이가 없는 것은, 고농도의 미백제로부터 충분한 활성 산소가 공급되어 착색 유기물이 대부분 제거되었기 때문에 수증기 첨가에 따른 플라즈마의 효과가 유의하게 나타나지 않은 것으로 사료된다. 3차 미백 처치가 완료된 후의 ΔE*값을 비교하였을 때, 15BPH, 35BP 및 35BPH 간의 유의한 차이가 나타나지 않았다(p>0.05). 그러므로 환자의 민감도와 같은 문제로 35 %의 미백제를 적용하기 곤란한 경우 15 %의 미백제를 수증기 첨가 플라즈마와 함께 적용한다면 충분히 고농도에 준하는 효과를 얻을 수 있을 것으로 기대된다. 다만 수증기의 농도가 높을수록 미백 효과가 좋은 것은 아니며, 너무 과도한 수증기가 함유될 경우 감전 혹은 플라즈마의 효과가 감소될 수 있으므로 1중량% 미만을 적용하여야 한다(Choi 등, 2015). 또한 기존의 치아 표면이 젖어 있을 경우 같은 원리로 플라즈마의 미백 효과가 증진될 수 있다. 그러나 미백제의 젤이 도포 위치에서 유동적으로 움직일 가능성이 있고 표면의 수분이 미백제의 농도에 영향을 줄 수 있으므로, 방전 가스에 수증기를 첨가하여 미백 효과를 개선하는 방법이 보다 합리적일 것으로 사료된다.
3) NBS 단위에 따른 미백 효과 판정
임상에서 육안으로 색지수 변화를 판별하기 위해서는 ΔE*값이 최소 3.3 이상이어야 하며(Johnston과 Kao, 1977; Ruyter 등, 1987), 그 값이 8을 초과할 경우 보다 즉각적으로 인지할 수 있다(Gross와 Moser, 1977). 이렇게 육안으로 판별 가능한 색지수 변화의 정도는 ΔE*값을 기반으로 단계화한 NBS 단위로 환산하여 Table 4에 나타내었다. NBS 단위 값에 따라 총 6단계로 분류하며, 미백 처치 전과 비교하였을 때 그 값이 6 이상 12 미만일 경우 ‘much’로, 12 이상일 때는 ‘very much’로 표현하였다. 본 실험 결과 시 5 %의 HP를 단독 적용한 5B 경우 1차, 2차, 3차 미백에서 NBS 단위 값이 6.5, 8.4, 11.1로 육안으로 판별 가능한 수준인 ‘much’로 판단하였다. 반면에 조건을 달리하여 플라즈마를 적용한 5BP, 5BPH는 모두 12 이상의 높은 값을 나타내어 ‘very much’로 판정하였다. 따라서 5 %의 HP를 적용하여도 플라즈마를 추가로 조사한다면, 1회 미백처치 후에도 환자가 즉각적으로 색조 개선을 인지할 수 있을 것으로 예상된다. 15 %의 HP를 적용하였을 때 15B, 15BP, 15BPH의 모든 미백 처리 단계에서 모두 13 이상의 높은 값을 가졌다. 35 %의 HP를 적용 시 35B는 14에서 19 사이, 35BP와 35BPH는 최소 18 이상의 값을 나타냈다. 이처럼 15 % 이상의 HP 농도에서는 미백 처리 방법에 상관없이 모두 육안으로도 현저히 색조가 개선됨을 판단할 수 있는 ‘very much’에 해당되는 미백 효과를 나타냄을 알 수 있다.
본 연구를 위해 우전치를 선별하는 과정에서 초기 L*값과 착색 후 L*값이 유사한 시편을 선별하였으나, 각 치아 시편 간 특성 차이로 인한 오차가 존재하였을 것으로 예상된다. 또한 위 미백 처치 방법을 임상적으로 적용 시 개인의 치아 특성 및 구강 내 환경으로 인한 차이를 감안해야할 것이다. 이러한 점을 보완하여 미백제에 수증기 첨가 플라즈마를 적용함에 따른 치아 표면의 물성 변화, 주위 조직에 대한 생물학적 안전성 및 장기적인 지속 효과 등에 대한 추가적인 연구가 진행되어야 할 것으로 보인다.
지금까지의 결과를 종합하였을 때, 5 % 및 15 % HP의 3차 미백 처치 시 B, BP, BPH 순서로 유의한 ΔE*값의 증가를 보였다(p<0.05). 35 % HP의 3차 미백 처치 시 35B 보다 35BP 및 35BPH에서 ΔE*값이 유의하게 증가하였으나(p<0.05), 35BP 및 35BPH 간의 유의한 차이는 없었다(p>0.05). 또한 15BPH는 35BP 및 35BPH와 ΔE*값의 유의한 차이가 없었다(p>0.05). 따라서 앞으로 조작 및 휴대가 간편하게 개선된 플라즈마 장비를 임상 및 가정에 보급하여 15 % 이하의 HP와 함께 적용한다면, 고농도의 위험을 감수하지 않고도 충분히 만족스러운 색조 개선 효과를 볼 수 있을 것으로 기대된다.
Ⅳ. CONCLUSION
본 연구는 우전치에 농도별 HP를 단독 도포하거나 플라즈마 또는 미량의 수증기를 첨가한 플라즈마 조사에 따른 미백 효과를 확인하고자 하였다. 미백을 총 3회 시행한 후 색조변화량(ΔE*) 및 NBS 단위 값에 따라 평가하였으며 그 결과는 다음과 같다.
- 1. 3차 미백 처치 시 미백 전에 비해 모든 군에서 ΔE*값이 유의하게 증가하였다(p<0.05).
- 2. 5 %, 15 % HP의 3차 미백 처치 시 단일 HP 군, 플라즈마 군, 수증기 첨가 플라즈마 군 순서로 ΔE*값이 유의하게 증가하였다(p<0.05).
- 3. 35 % HP의 3차 미백 처치 시 단일 HP 군에 비해 플라즈마 군 및 수증기 첨가 플라즈마 군에서 ΔE*값이 유의하게 증가하였으며(p<0.05), 두 군 간의 유의한 차이는 없었다(p>0.05).
- 4. 3차 미백 처치 시 15 % HP 수증기 첨가 플라즈마 군은 35 % 플라즈마 및 35 % 수증기 첨가 플라즈마 군과 ΔE*값의 유의한 차이가 없었다(p>0.05).
본 실험에서 수증기를 첨가한 플라즈마를 조사할 경우 미백 효과를 향상시킬 수 있었으며, 이를 15 % HP에 적용했을 때 35 % HP의 적용에 상응하는 결과를 보임으로써, 보다 안전하면서도 효과적인 차세대 미백 치료의 기초 자료로서 활용될 것으로 기대된다.
Acknowledgments
* 이 논문은 2010년도 정부(미래창조과학부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(No. NRF-2010-0027963).
Ⅴ. REFERENCES
- Choi, EH., Kim, KN., Kim, YH., Kwon, JS., (2015), Removing method of tooth cell coloring material with plasma, Korea Patent Application 10-1500155.
-
Gross, MD., Moser, JB., (1977), A colorimetric study of coffee and tea staining of four composite resins, J Oral Rehabil, 4, p311-322.
[https://doi.org/10.1111/j.1365-2842.1977.tb00997.x]

- Harlan, AW., (1884), The removal of stains from teeth caused by administration of medical agents and the bleaching of pulpless tooth, Am J Dent Sci, 18(521), p355-61.
-
Haywood, VB., (2002), Dentin hypersensitivity bleaching and restorative considerations for successful management, Int Dent J, 52, p7-10.
[https://doi.org/10.1002/j.1875-595X.2002.tb00937.x]

- Heithersay, GS., (1999), Invasive cervical resorption: analysis of potential predisposing factors, Quintessence Int, 30, p83-95.
-
Johnston, WM., Kao, EC., (1987), Assessment of appearance match by visual observation and clinical colorimetry, J Dent Res, 68, p819-822.
[https://doi.org/10.1177/00220345890680051301]

-
Joiner, A., (2004), Tooth colour: a review of the literature, J Dent, 32(Suppl.1), p3-12.
[https://doi.org/10.1016/j.jdent.2003.10.013]

-
Joiner, A., (2006), The bleaching of teeth: A review of the literature, J Dent, 34, p412-419.
[https://doi.org/10.1016/j.jdent.2006.02.002]

-
Kawamoto, K., Tsujimoto, Y., (2004), Effects of the Hydroxyl Radical and Hydrogen Peroxide on Tooth Bleaching, J Endodont, 30(1), p45-50.
[https://doi.org/10.1097/00004770-200401000-00010]

-
Lee, HW., Kim, GJ., Kim, JM., Park, JK., Lee, JK., Kim, GC., (2009), Tooth bleaching with nonthermal atmospheric pressure plasma, J Endod, 35, p587-591.
[https://doi.org/10.1016/j.joen.2009.01.008]

-
Lenhard, M., (1996), Assessing tooth color change after repeated bleaching in vitro with a 10 percent carbamide peroxide gel, J Am Dent Assoc, 127(11), p1618-1624.
[https://doi.org/10.14219/jada.archive.1996.0097]

- Leonard, RH., Sharma, A., Haywood, VB., (1998), Use of different concentration of carbamide peroxide for bleaching teeth: an in vitro study, Quintessence Int, 29(8), p503-507.
-
Moraes, RR., Marimon, JLM., Schneider, LFJ., Sobrinho, LC., Camacho, GB., Bueno, M., (2006), Carbamide peroxide bleaching agents: effects on surface roughness of enamel, composite and porcelain, Clin Oral Investig, 10, p23-28.
[https://doi.org/10.1007/s00784-005-0016-1]

-
Naik, S., Tredwin, CJ., Scully, C., (2006), Hydrogen peroxide tooth-whitening (bleaching): review of safety in relation to possible carcinogenesis, Oral Oncol, 42, p668-74.
[https://doi.org/10.1016/j.oraloncology.2005.10.020]

-
Ruyter, IE., Niler, K., Moller, B., (1987), Color stability of dental composite resin materials for crown and bridge veneers, Dent Mater, 3, p246-251.
[https://doi.org/10.1016/S0109-5641(87)80081-7]

-
Shotwell, JL., Razzoog, ME., (1992), Color stability of long-term soft denture liners, J Prosthet Dent, 68, p836-838.
[https://doi.org/10.1016/0022-3913(92)90213-T]

-
Stookey, GK., Burhard, TA., Schemehorn, BR., (1982), In vitro removal of stain with dentifrices, J Dent Res, 11, p1236-9.
[https://doi.org/10.1177/00220345820610110501]

- Tavares, M., Stultz, J., Newman, M., Smith, V., Kent, R., Carpino, E., (2003), Light augments tooth whitrning with peroxide, J Am Dent Assoc, 134(2), p167,175-.