지각과민처치제가 초음파 스케일링 처리한 비우식성 치경부 병소가 있는 치아의 지각과민증에 주는 영향
Abstract
The aim of this study was to evaluate the changes in dentinal permeability after application of dentin desensitizer on exposed dentin immediately after ultrasonic scaling to teeth with non-carious cervical lesions. Thirty caries-free extracted molars were fixed to slide glasses after horizontally being sectioned at 5 mm below the cemento- enamel junction (CEJ). The prepared specimen was connected to a fluid flow measuring device (nano-Flow), and a V-shaped cavity was formed at the CEJ to imitate the non-carious cervical lesion. After no fluid leakage was confirmed in the connected system with specimen, tooth surface was treated ultrasonic cleaning with piezoelectric ultrasonic scalers until dentinal tubules were exposed. And 6 different desensitizers were applied on exposed dentin. Real-time measurements of dentinal fluid flow were performed during ultrasonic scaling and application of dentin desensitizer. To evaluate the occlusion of exposed dentinal tubules, tooth surface was examined by SEM. Following results were observed. After ultrasonic scaling, more dentinal tubules were exposed on the tooth with non-carious cervical lesions compared to tooth without lesions. The rate of fluid flow measured with nano-Flow system had correlation with the degree of dentin occlusion observed with SEM after application of desensitizers on exposed dentin. Desensitizers with glutaraldehyde and HEMA did not decrease the rate of fluid flow and did not show dentin occlusion. Desensitizers with oxalate showed the limited effects on the rate of fluid flow and dentinal tubule occlusion. Desensitizer with resin monomer showed the significant effect on the rate of fluid flow and dentin occlusion.
Keywords:
Desensitizing Agent, Non-carious Cervical Lesions, Ultrasonic Scaling, Dentin, Real-time Measurement of Dentinal Fluid FlowⅠ. INTRODUCTION
2013 년부터 스케일링에 대한 건강보험이 적용되면서 스케일링 환자가 크게 증가하고 있는데, 스케일링을 받은 환자들이 자주 지각과민증 (hypersensitivity)을 호소하고 있다. 상아질 지각과민증이란 치아의 손상이나 질병에 의한 통증이 아니라 정상적인 치아에서 열, 기화, 삼투압, 화학물질 및 접촉 등의 외부 자극에 의해 발생하는 짧고 강한 통증으로 정의하고 있다 (Jacobsen과 Bruce, 2001; Walters, 2005; Mantzourani와 Sharma, 2013). 이러한 지각과민증은 임상에서 환자들이 주로 호소하는 주소 (chief complain)의 하나로 완치가 힘든 치과 질환이다. 치주 치료를 받는 환자의 8-35%에서 치경부 지각과민증이 유발되었다고 하였는데 (Chabanski 등, 1997), 치료 환자의 34.2% 정도에서 제기된 지각과민증은 치주 수술 후의 합병증 중에서 가장 높은 빈도를 보였다고 하였다 (신 등, 1988).
상아질 지각과민증이 발현되는 기전으로 노출된 상아질에서 외부 자극에 의한 상아세관 내 액체 이동 변화는 조상아 세포, 신경말단 또는 혈관 등을 자극하여 통증이 유발된다는 유체역학 (hydrodynamic) 이론이 일반적으로 받아들여지고 있다 (Brännström 등, 1967). 지각과민증을 유발할 수 있는 상아질 노출은 잘못된 잇솔질 방법에 의한 만성적 외상, 환경에 의한 산-침식 (erosion), 위산 역류 또는 식습관, 백아법랑 경계의 해부학적 요인, 수복 치료시의 치아삭제 및 치주질환이나 치주 수술로 인한 치은 퇴축에 따른 치근 표면의 노출 등에 의해 나타날 수 있다 (Addy 등, 1994). 치아 우식증에 의하지 않고 법랑질 두께가 가장 얇은 치경부의 백악-법랑 경계부위에서 구조적 결함이 생성되는 것을 비우식성 치경부 병소라고 한다. 이렇게 형성된 병소는 지각과민증을 유발하거나 치태 침착이 집중되어 치아 우식증 발생을 증가시키는 요인이 될 수도 있다 (Piotrowski 등, 2001). Grippo (1992)는 비우식성 치경부 병소 생성에 영향을 줄 수 있는 요인으로 마모 (abrasion)와 침식 뿐 아니라 굴곡파절 (abfraction)도 중요한 역할을 한다고 하였다.
높은 상아질 투과성 (permeability)으로 지각과민증이 발현되는 상아질은 상아세관의 투과도를 감소시키거나 완전히 소멸시킬 경우 이론적으로 지각과민증 증상이 감소되거나 소멸되어야 한다 (Pashley, 1984; Pashley, 1986). Haugen과 Johansen (1988)은 치주 수술 후에 지각과민증을 호소하는 환자의 치아를 주사전자현미경 (SEM)으로 관찰하여 상아세관이 노출된 것을 확인하였고, Yoshiyama 등 (1989)은 SEM으로 관찰한 결과 지각과민증이 발병된 상아질은 상아세관이 노출되어 있었으나, 자연적으로 탈감작 (desensitization)된 상아질에서는 상아세관이 수산화인회석 결정 등으로 봉쇄된 것이 관찰되었다고 하였다. 현재 상아질 지각과민증 치료를 위하여 신경의 탈분극을 유도하는 포타슘 이온 (K+) 농도를 증가시켜 자극에 대한 치수 내 감각 신경의 흥분을 억제하는 방법이나 열린 상아세관을 봉쇄시켜 상아세액의 이동을 차단하는 방법이 적용되고 있다 (Orchardson과 Gillam, 2006; Bamise와 Esan, 2011; 조 등, 2014). 임상에서 주로 사용되는 지각과민처치제 (desensitizer)는 상아질 표면의 밀폐, 상아세액의 단백질 침착 및 칼슘 복합체 형성 등으로 상아세관을 봉쇄하거나 노출된 상아세관의 지름을 감소하는 방법으로 상아세액 이동을 억제시켜 지각과민증을 완화시키고 있다.
외부 자극에 의해 유발된 상아세관 내 액체 흐름의 변화는 상아질 지각과민증의 통증을 유발하는 중요한 원인이므로 그 흐름의 변화를 관찰하는 것은 다양한 탈감작 방법, 지각과민처치제에 의한 상아세관의 봉쇄 및 지각과민증 완화 효과 등의 예측에 중요한 역할을 할 수 있다. Kim 등 (2010)은 발치된 치아를 사용하여 아말감 또는 컴포짓트 레진으로 수복하는 과정 중 상아세액의 흐름을 실시간으로 측정한 연구를 보고하였고, Kim 등 (2013)은 지각과민처치제 적용에 따른 상아세관 봉쇄 정도를 실시간으로 측정한 연구 결과를 보고하였는데, 이들의 연구에서는 0.2 nL의 해상도로 상아세관을 통한 물의 흐름을 실시간으로 측정하였다. 현재까지 다양한 조건에서 상아질 투과성을 측정한 연구 결과들이 많이 보고되었으나 (Hoang-Dao 등, 2008; Komabayashi 등, 2010; Mitchell 등, 2011; Patel 등, 2011), 초음파 스케일링 처리에 따른 상아세관의 노출 가능성을 실시간으로 측정한 연구는 거의 없는 상황이다. 본 논문에서는 인위적으로 비우식성 치경부 병소를 생성한 치아를 대상으로 초음파 스케일링 처리하는 과정에서 상아세관의 노출 가능성을 실시간으로 측정하고, 상아세관이 노출된 경우 지각과민처치제를 도포하여 상아세관 봉쇄능 효과를 실시간으로 평가하고자 하였다.
Ⅱ. MATERIALS AND METHODS
1. 연구재료
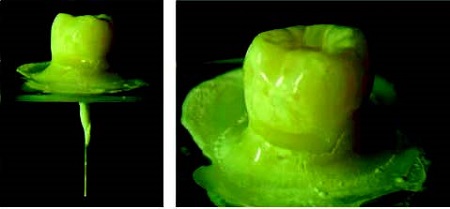
우식 및 수복물이 없는 발치된 소구치와 대구치 30 개를 백악-법랑 경계 하방 5 mm 부근에서 저속 다아아몬드 톱 (low speed diamond saw; Isomet, Buehler, USA)으로 치아를 절단하였고, 절단한 치아의 전상아질 (predentin)이 손상되지 않도록 가느다란 근관치료용 파일과 탐침을 이용하여 치수를 제거하였다. 슬라이드 글라스 양면을 샌드블라스팅 처리하고 절단한 치아 시편과 물 (deionized water) 저장고 (reservoir)를 연결하기 위한 0.9 mm 지름의 구멍을 뚫어 치수강에 금속 튜브를 삽입하고 레진 접착제 (Clear Protect Bond, Kuraray Medical Inc, Japan)와 유동형 컴포짓트 레진 (Heliomolar Flow, Ivoclar Vivadent, Liechtenstein)을 이용하여 금속 튜브를 연결한 치아를 슬라이드 글라스에 접착하였다. 연결한 금속 튜브 외에서 발생할 수 있는 미세누출을 방지하기 위하여 노출된 치근면과 치아-슬라이드 글라스 접촉면 외부를 투명한 네일 바니쉬 (nail varnish)로 밀봉하였다 (Fig. 1).
준비가 완료된 시편은 흐름성 측정 장치 (nano-Flow, IB Systems, Seoul, Korea)에 연결하고 20 ㎝‧H2O의 정수압을 가하여 누출되는 부분이 없는지 확인하였고, 4℃로 냉각한 물과 60℃로 가열한 물을 시편 외부에 적시며 측정 장치의 정상적인 반응을 확인하였다. 미세한 누출 경향을 보이거나 외부 온도 변화에 적절한 반응을 보이지 않는 시편은 실험에서 제외시켰다. 건전한 치아에 인위적으로 비우식성 치경부 병소를 생성하기 위하여 치경부의 백악-법랑 경계 (CEJ) 부근에 근원심으로 V 형 (길이 5 mm × 높이 2 mm × 깊이 1 mm) 와동을 고속 핸드피스와 다이아몬드 버로 형성하였다. 비우식성 치경부 병소를 형성한 시편을 흐름성 측정장치에 연결하고 정수압을 가하여 안정화시킨 다음 비우식성 치경부 병소 형성에 따른 상아세관 노출 여부를 확인하여 누출되지 않은 시편만 실험군으로 사용하였는데, 6 개 실험군에 4 개씩 모두 24 개의 시편을 준비하였고, 대조군으로 건전한 시편 4개를 사용하였다.
초음파 스케일링으로 노출된 상아질에 적용하여 상아세관 봉쇄 정도를 평가하기 위하여 6 종의 지각과민처지제를 사용하였다 (Table 1). Glutaraldehyde를 주성분으로 하는 제품 2 종 (Gluma Desensitizer, MicroPrime G), oxalate를 주성분으로 하는 제품 3 종 (SuperSeal, BisBlock, MS-Coat One), 기능성 단량체 등을 함유한 Seal & Protect 등 6 종을 시험하였다.
2. 연구방법
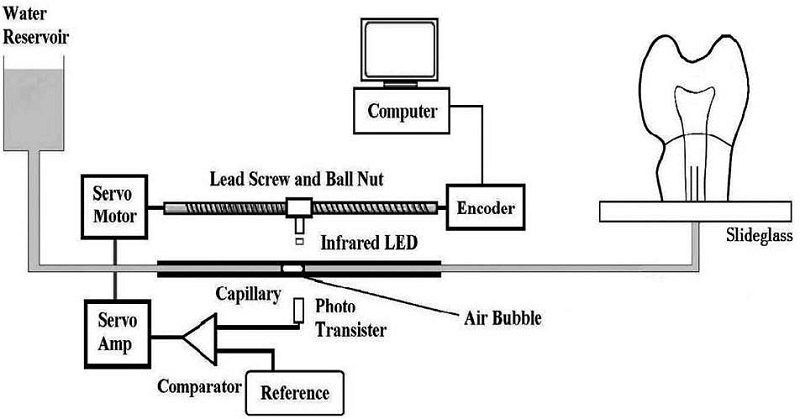
상아세관내 액체의 미세한 흐름을 측정하기 위하여 나노 물 흐름 측정장치 (nano-Flow, IB Systems, Seoul, Korea)를 사용하였는데, 물의 흐름을 감지하는 유리 모세관과 광센서, 물의 흐름을 추적하는 서보 모터, 엄지 나사 (lead screw)와 볼 너트 (ball nut), 데이터를 기록하는 회전 인코더 및 컴퓨터 소프트웨어 등으로 구성되어 있다 (Fig. 2). 물 저장고와 치아 시편 사이에 연결되어 증류수로 채워져 있는 내경 0.5 mm의 유리 모세관 안에는 공기방울이 함입되어 있으며, 유리관 내 물의 흐름에 따라 공기방울이 이동하게 되면 적외선 방출 다이오드와 광트랜지스터로 구성된 광센서에 의해 감지되고, 광센서가 물-공기 계면을 계속 추적할 수 있도록 서보앰프와 서보모터는 엄지나사를 회전시킨다. 나사의 회전은 회전 인코더를 통해 1,000 개/회전의 펄스로 감지되어 컴퓨터에 기록되어 저장되는데, 측정 장치의 최소 측정량은 0.196 nL로 미세한 흐름 변화를 측정할 수 있다.
비우식성 치경부 병소를 형성한 시편을 물 흐름 측정장치에 연결하고 정수압을 가하여 안정화시킨 다음 5-10 분간 상아세관을 통한 물의 흐름을 측정하여 기준값으로 정하였다. 초음파 스케일링은 압전방식 (piezoelectric)인 Mini Piezon Dental Ultrasonic Scaler (EMS-SCAL04, Electro Medical Systems, Swiss)를 이용하였다. 비우식성 치경부 병소를 형성하지 않은 결함이 없는 건전한 치아 시편과 비우식성 치경부 병소를 형성한 치아 시편을 대상으로 치수강 내 액체의 흐름성을 실시간으로 측정하면서 치아 표면을 초음파 스케일러로 스케일링 처리하여 비우식 치경부 병소 유‧무에 따른 초음파 스케일러 처리 효과를 비교하였고, 흐름율이 증가하는 양상이 관찰되면 초음파 스케일링은 중단하였다.
흐름성 측정 장치에 연결한 후 초음파 스케일링 처리하여 흐름율이 증가되는 양상을 보인 시편은 스케일링 처리 과정에서 노출된 상아질 표면에 지각과민처치제를 제조사의 설명서에 따라 도포하였다. 제품에 따라 광중합이 필요한 경우 LED 광조사기 (Elipar S10, 3M ESPE)로 광조사하였다. 지각과민처치제 적용 등 모든 과정에서 시편 내에서의 물 흐름 변화는 실시간으로 측정하여 컴퓨터로 기록하였다.
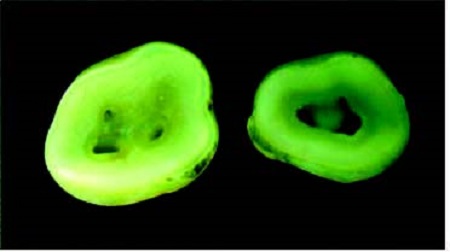
흐름성 측정이 완료된 시편을 상아질이 노출되도록 저속다이아몬드 톱 (low speed diamond saw; Isomet, Buehler, USA)으로 치아의 치관부를 제거하고 2 mm 두께로 절단하였다 (Fig. 3). 노출된 상아질을 35% 인산 (Vericom, USA)으로 5 초간 산-부식 처리한 후 물로 세척하였다. 상아질 표면에 6 종의 지각과민처치제를 제조사의 설명서에 따라 적용한 다음 37℃ (100% 상대 습도)에서 2 시간 유지하여 지각과민처치제가 상아질 표면에서 적절한 반응할 수 있도록 하였다. 지각과민처치제를 도포하지 않은 대조군과 지각과민처치제를 도포한 상아질 시편의 표면을 OsO4로 코팅한 다음 FE-SEM (S-4700, Hitachi, Japan)으로 상아세관을 관찰하여 지각과민처치제가 상아세관을 봉쇄하는 정도를 분석하였다.
Ⅲ. RESULTS
Fig. 4는 비우식성 치경부 병소를 인위적으로 형성한 시편에 초음파 스케일링 처리 과정에서 증류수의 흐름율이 급격히 증가되는 시점으로 상아세관 노출을 인지하고, 지각과민처치제인 Gluma Desensitizer를 도포하면서 시편 내부에서의 증류수 흐름율 변화를 실시간으로 관찰한 결과를 나타낸 그래프이다. 노출된 상아질 부위에 glutaraldehyde와 HEMA가 주 성분인 Gluma Desensitizer를 적용하여도 증류수 흐름율은 감소되지 않아서 상아세관은 봉쇄되지 못한 것으로 보였다. Fig. 5는 Gluma Desensitizer와 유사하게 glutaraldehyde와 HEMA를 주성분으로 하는 MicroPrime G 지각과민처치제를 노출된 상아질에 적용하여 봉쇄 효과를 실시간으로 관찰한 그래프이다. 측정 결과는 Gluma Desensitizer를 적용한 경우와 유사하였으며, MicroPrime G 지각과민처치제 경우에서도 상아세관 봉쇄 효과는 관찰되지 않았다.
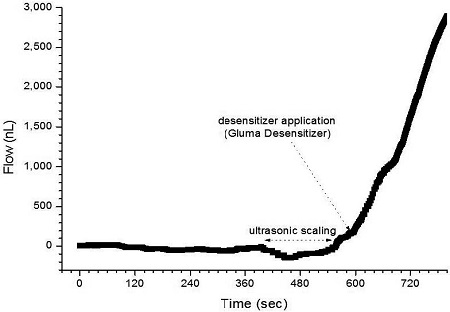
Dentinal fluid flow curve as a function of time with Gluma Desensitizer application subsequent to ultrasonic scaling treatment.
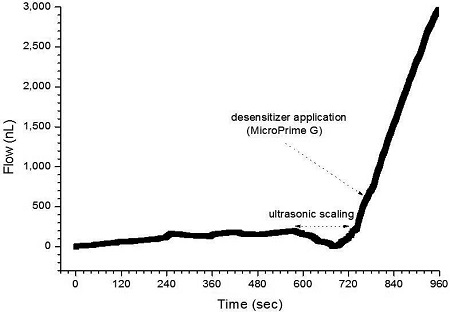
Dentinal fluid flow curve as a function of time with MicroPrime G application subsequent to ultrasonic scaling treatment.
Fig. 6은 초음파 스케일링 처리로 상아세관이 노출된 부위에 SuperSeal 지각과민처치제를 적용하고 증류수의 흐름율 변화를 실시간으로 관찰한 결과를 기록한 그래프이다. Oxalic acid와 포타슘 염이 주성분인 SuperSeal 지각과민처치제는 glutaraldehyde가 주성분인 지각과민처치제들과 마찬가지로 상아세관이 노출된 부위에 적용하여도 즉각적인 상아세관 봉쇄 효과는 볼 수 없었지만, 780 초 부근에서 증류수 흐름율이 다소 감소되는 양상이 관찰되어 완전하지는 않지만 적은 상아세관 봉쇄 효과가 있음을 알 수 있었다. Fig. 7에는 oxalic acid와 포타슘 염을 주성분으로 하는 SuperSeal과 유사하지만 추가로 접착제가 포함된 BisBlock 지각과민처치제의 적용 효과를 실시간으로 관찰한 그래프이다. 레진 성분이 없는 SuperSeal과는 다르게 640 초 부근에서 증류수 흐름율 감소가 더 명확하게 관찰되어 지각과민처치제 도포에 따른 상아세관 봉쇄 효과가 있음을 알 수 있었다. Fig. 8은 oxalic acid를 주성분으로 하는 MS-Coat One 지각과민처치제를 상아세관이 노출된 부위에 적용하고 상아세관 봉쇄 효과를 실시간으로 관찰한 그래프이다. Oxalate를 주성분으로 하는 SuperSeal 또는 BisBlock 지각과민처치제와는 상이하게 노출된 상아질에 적용하여도 증류수 흐름율 감소가 전혀 관찰되지 않으므로 상아세관 봉쇄 효과는 거의 없는 것으로 보였다.
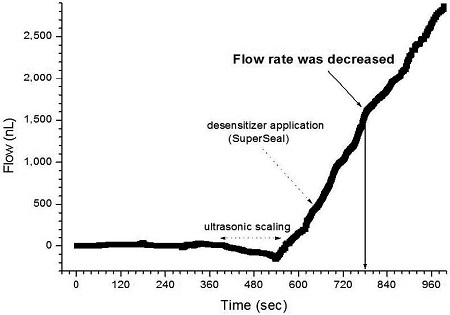
Dentinal fluid flow curve as a function of time with SuperSeal application subsequent to ultrasonic scaling treatment.
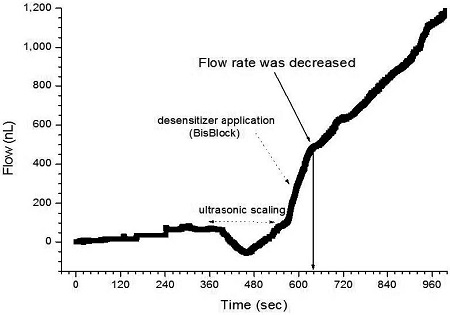
Dentinal fluid flow curve as a function of time with BisBlock application subsequent to ultrasonic scaling treatment.
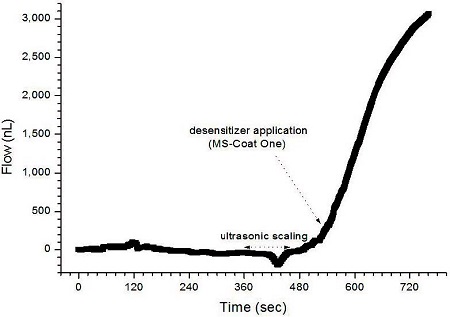
Dentinal fluid flow curve as a function of time with MS-Coat One application subsequent to ultrasonic scaling treatment.
Fig. 9에는 필러를 함유한 레진과 기능성 단량체 (PENTA)가 주성분인 Seal & Protect 지각과민처치제를 상아세관이 노출된 부위에 적용하고 상아세관 봉쇄 효과를 실시간으로 관찰한 그래프이다. 다른 지각과민처치제를 적용한 실험군과 달리 530 초 부근에서 증류수 흐름율 감소가 명확하게 관찰되어 상아세관 봉쇄 효과를 볼 수 있었다.
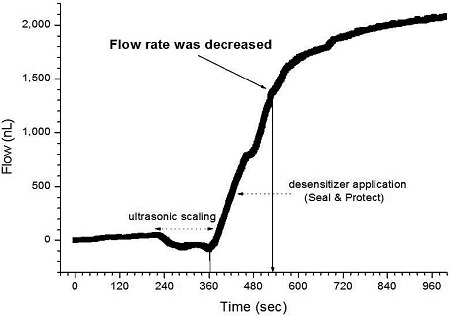
Dentinal fluid flow curve as a function of time with Seal & Protect application subsequent to ultrasonic scaling treatment.
Figs. 10-12은 산-부식처리한 상아질 표면에 6 종의 지각과민처치제를 적용하고 37℃ (100% RH)에서 2 시간 유지시킨 다음 주사전자현미경으로 상아질 표면을 관찰한 사진이다. Glutaraldehyde와 HEMA가 주성분인 Gluma Desensitzer를 적용한 경우에는 상아세관의 아주 적은 부분만 불완전하게 봉쇄되어 있는 것으로 관찰되었다 (Fig. 10a). 유사한 성분으로 구성된 MicroPrime G의 경우도 Gluma Desensitzer와 유사한 정도로 상아세관을 부분적인 불완전 봉쇄를 보였다 (Fig. 10b).

SEM images of dentin surface after desensitizer application subsequent to acid-etching: (a) Gluma Desensitizer, and (b) MicroPrime G.
Oxalate가 주성분인 SuperSeal (Fig. 11a), BisBlock (Fig. 11b) 및 MS-Coat One (Fig. 11c)을 적용한 경우에는 상아질 표면에 옥살레이트 결정상이 형성된 것이 관찰되었으며, Gluma Desensitizer 또는 Micro Prime G를 적용한 경우 보다는 더 많은 상아세관 봉쇄정도를 보였다. 레진 단량체와 필러가 주성분인 Seal & Protect을 적용한 경우 상아질 표면은 레진 피막으로 덮여 있었으며, 일부분 상아세관이 노출된 곳도 관찰되었다(Fig. 12).

SEM images of dentin surface after desensitizer application subsequent to acid-etching: (a) SuperSeal, (b) BisBlock, and (c) MS-Coat One.
Ⅳ. DISCUSSION
본 연구에서는 인위적으로 비우식성 치경부 병소를 생성한 치아를 대상으로 초음파 스케일링 처리하는 과정에서 상아세관의 노출 가능성을 실시간으로 확인할 수 있었으며, 상아세관이 노출된 경우 적절한 지각과민처치제를 도포하여 상아세관의 봉쇄 효과를 관찰할 수 있었다.
치면에 부착된 치태 및 치석은 백악질을 변성 또는 연화시킬 수 있으며, 치태와 치석이 치주질환 유발의 중요한 원인이므로 치석 제거는 구강건강 유지를 위해 반드시 필요하다. Wolff (2009)는 치면에 부착된 치태와 치석 등과 같은 바이오 필름 (biofilm) 생성이 지각과민증과의 직접적인 상관성은 없다고 하였지만, 치석 제거 과정에서 상아질이 삭제되어 상아세관 노출이 유도되는 경우 지각과민증에 의한 동통이 유발될 가능성은 매우 높다. 특히 법랑질 층의 두께가 가장 얇은 치경부 부위에서는 침식, 마모 및 굴곡파절 등에 의해 법랑질이 쉽게 파괴될 수 있기 때문에 상아질 노출이나 치수 노출 가능성도 매우 높아 (Lee와 Eakle, 1996; West, 2008) 치경부 지각과민증은 흔하게 보고되고 있는데, 성인의 15-74%에서 관찰되고 있다고 한다 (Ritter 등, 2006; Udoye, 2006; Terry, 2011; Que 등, 2013). 특히, 비우식성 치경부 마모증과 치경부 지각과민증은 치아의 동일한 부위에서 관찰되며 상호 밀접한 상관성이 있다고 보고되었다 (Bartlett와 Shah, 2006; Que 등, 2011).
Gluma Desensitizer는 HEMA와 결합된 glutaraldehyde가 상아세관 내부로 깊숙히 침투하여 상아세액 단백질과 침착물을 형성함으로써 상아세관을 봉쇄할 수 있다고 한다 (Felton 등, 1991; Ritter 등, 2000; Kakaboura 등, 2005). 하지만 본 연구에서는 Gluma Desensitizer의 상아세관 봉쇄효과가 전혀 관찰되지 않는 상반된 결과가 관찰되었는데, 본 연구에서 사용한 치아의 경우 시편 제작과정에서 glutaraldehyde와 결합할 수 있는 단백질이 모두 제거되어 상아세관 봉쇄를 위한 반응물질이 전혀 잔류하지 못한 것 때문으로 추정하였다. 또한, Gluma Desensitizer와 유사한 성분으로 구성된 MicroPrime G를 적용한 경우에서도 상아세관 봉쇄효과는 관찰되지 않았다. Ishihata 등 (2012)은 glutaraldehyde 함유 지각과민처치제의 상아질 투과도 감소 효과를 평가한 결과 우수한 감소효과가 관찰되었다고 하였는데, 시편 제작 후 2% bovine albumin 용액을 적용한 다음 투과율을 측정했기 때문에 glutaraldehyde가 bovine albumin과 반응하여 침착물 형성이 가능하여 봉쇄 효과가 관찰된 것으로 보였다.
Dijkman 등 (1994)은 EDTA와 2% glutardialdehyde로 처리한 상아세관의 봉쇄효과를 SEM으로 분석한 연구에서 glutardialdehyde는 도말층 (smear layer)과 superficial dentinal 표면을 고정할 수 있으며 상아세관을 봉쇄시킬 수 있다고 하였다. Schüpbach 등 (1997)은 다양한 유형의 Gluma Desensitzer (Gluma 2 Cleanser, Gluma 3 Primer, Gluma 4 Sealer) 적용에 따른 상아세관 봉쇄효과를 SEM, TEM 및 CLSM (fluorescence confocal laser scanning microscopy)로 분석한 결과 Gluma 3 Primer를 적용한 경우에만 우수한 상아세관 봉쇄효과가 관찰되었다고 하였다. Glutaraldehyde와 HEMA로 구성된 Gluma의 임상 효용성과 관련된 문헌들을 분석한 연구에서 Gluma는 지각과민증 감소에 효과적이고, 산-부식처리한 치아 표면의 적심성을 향상시켜 접착력을 증가시킬 수 있을 뿐 아니라 우식이 있는 상아질 부위에 적용할 경우 항우식 효과도 기대할 수 있다고 하였다 (Boksman과 Swift, 2011; Larson, 2013). 반면, de Assis 등 (2006)은 치주질환 치료를 실시한 환자에게 Gluma Desensitizer를 적용한 다음 4 주간 영향을 평가한 결과 지각과민증이 감소된 결과는 관찰되지 않았다고 하는 상반된 결과를 보고하였다.
Oxalate를 함유한 지각과민처치제는 상아질 표면의 칼슘이온과 반응하여 칼슘 oxalate 불용성 침착물을 형성하여 상아세관을 봉쇄할 수 있다. 옥살산염이 효과적으로 상아세관을 봉쇄할 수 있지만, 표면에 형성된 침착물이 타액에 쉽게 용해될 수 있기 때문에 지속적인 상아세관 봉쇄를 위하여 주기적으로 반복해서 도포해야 한다고 한다. SuperSeal과 BisBlock의 경우는 친수성인 포타슘 oxalate가 노출된 상아세관에서 칼슘 oxalate 침착물을 형성하여 상아세관을 봉쇄할 수 있으며, oxalic acid는 도말층 제거뿐 아니라 포타슘 oxalate가 상아세관내부 깊은 부위까지 침투할 수 있도록 도움을 준다고 하였다 (Pashley와 Galloway, 1985). MS-Coat One은 oxalic acid, polystyrene sulfonic acid, PMMA 및 레진 유화제 등을 함유하는 아크릴릭 레진과 수성 콜로이드 혼합물로 치질과 화학 반응으로 형성된 침착물이 상아질 세관을 봉쇄하여 외부 자극을 차단할 수 있다고 한다 (Pashley 등, 2001). Pillon 등 (2004)은 스케일링 또는 치근 활택술 후 상아질 지각과민증이 발생한 15 명의 환자에게 3% 포타슘 oxalate를 도포하고 7 일, 14일 및 21 일 경과한 후 완화 효과를 비교한 결과 3% 포타슘 oxalate가 지각과민증을 효과적으로 감소시켰다고 하였다. 그러나 Santiago 등 (2006)은 상용 제품 OxaGel과 실험용 포타슘 oxalate 지각과민처치제, placebo (carboxymethylcellulose gel) 및 증류수 등을 이용하여 상아질의 흐름율을 측정한 결과 상아질 투과도는 모든 실험군에서 시간경과에 따라 유의한 감소가 관찰되어 연구 결과를 분석할 때 유의하여야 한다고 하였다. Vieira 등 (2009b)도 지각과민증 환자 24 명에게 GaAlAs 레이저, 3% 포타슘 oxalate gel 및 placebo gel 등으로 처리하고 3 개월간 지각과민증 완화 효과를 관찰한 결과 모든 실험군에서 지각과민증 감소가 관찰되어 향후 장기간 효과에 대한 추가시험이 필요하다고 하였다.
Cunha-Cruz 등 (2011)은 2009 년 7 월까지 출간된 상아질 지각과민증 관련 677 개 문헌 중에서 임상 시험을 포함한 174 개 문헌에서 oxalate와 관련된 12 개 문헌을 분석한 결과 3% monohydrogen-monopotassium oxalate를 포함한 지각과민처치제를 제외한 다른 oxalate 성분으로 구성된 지각과민처치들은 상아질 지각과민증 완화효과가 거의 없이 placebo 제재와 유사한 정도였다고 하였다. 또한 7 개 문헌 분석으로 결론이 도출된 3% monohydrogen-monopotassium oxalate의 경우도 6 건의 문헌에서는 효과가 없거나 placebo보다 조금 유의한 효과를 보였다고 하였고, 단지 1 건의 문헌에서만 oxalate의 효과가 관찰되었다고 하였다. 따라서 oxalate가 상아질 지각과민증을 완화시킬 수 있다는 기존의 연구 결과에 다소 회의적이라고 하였다. 본 논문에서도 oxalate가 주요 성분인 지각과민처치제 (SuperSeal, BisBlock 및 MS-Coat One)를 적용한 실험군에서 상아세관 봉쇄효과가 기존에 발표된 연구만큼 크지 않은 것으로 관찰되었다. 따라서 de Andrade 등 (2007), Fu 등 (2007) 및 Barrientos 등 (2011)은 oxalate 함유 지각과민처치제 (Protect Drops, Oxagel, MS-Coat, BisBlock)로 상아질 표면을 처리할 경우에 상아질 접착제를 함께 적용하면 상아질 투과도를 크게 감소시킬 수 있으므로 지각과민증 완화를 위하여 상아질 접착제와 oxalate를 함께 적용하는 방법을 제시하였다.
항균 작용을 하는 triclosan, 기능성 단량체인 PENTA, methacrylate계 레진, 광개시제 및 필러 등으로 구성된 Seal & Protect는 자가-부식형 접착제와 유사한 방식으로 혼성층을 형성하여 상아세관 입구를 봉쇄하는 것으로 추정하고 있다. 여러 연구에서 Seal & Protect의 우수한 상아세관 차단 능력과 지각과민증 억제 효과가 보고되었는데 (Camps 등, 2002; Pamir 등, 2007), 본 논문에서도 평가한 지각과민처치제 중에서 Seal & Protect 실험군이 가장 우수한 상아세관 봉쇄효과가 관찰되었으며, 성분으로 함유된 레진 단량체들이 상아세관을 효과적으로 봉쇄하는 것으로 보였다.
Pamir 등 (2007)은 지각과민증 환자 60 명에게 Seal & Protect, Vivasens, BisBlock 및 placebo (증류수)를 적용하고 4 주 경과한 다음 지각과민증 완화 효과를 관찰한 연구에서 Seal & Protect, Vivasens 및 BisBlock을 적용한 경우는 증류수를 적용한 경우 보다 유의하게 지각과민증이 완화된 것이 관찰되었지만, 증류수도 유의할만한 지각과민증 완화효과를 보였다고 보고한 바 있다. Aranha 등 (2009)은 치경부 지각과민증 환자에게 Gluma Desensitizer, Seal & Protect, 3% 포타슘 oxalate gel인 Oxa-gel (Art Dent) 및 APF인 Nuprogel (Dentsply)를 적용하거나 저강도 (3.8 J/㎠/15 ㎽) GaAlAs 레이저 (MMOptics)로 치료한 다음 즉시, 1 주일, 1 개월, 3 개월 및 6 개월 경과한 시점에서 지각과민증의 완화 정도를 비교한 연구에서 Gluma Desensitizer 또는 Seal & Protect를 적용한 환자는 즉시 지각과민증 완화 효과가 관찰되었으며 효과는 6 개월간 지속되었다고 하였다. Oxa-gel을 적용한 환자는 1 개월 경과한 시점부터 지각과민증 완화가 관찰되었고, APF를 적용한 경우는 3 개월 경과한 시점부터 지각과민증 완화가 관찰되었다고 하였다. 반면 저강도 레이저로 치료한 환자는 지각과민증이 서서히 감소되는 양상을 보였고, 6 개월 경과한 시점에서는 5 개 실험군 모두에서 지각과민증 완화효과는 유의한 차이 없이 유사하였다고 발표하였다.
Yu 등 (2010)은 지각과민처치제 (Gluma Desensitizer)와 자가부식형 접착제 (iBond, Xeno V), 불소제재 (Bifluorid 12) 및 placebo (증류수)의 지각과민증 완화 효과를 비교한 결과 지각과민처치제와 자가부식형 접착제는 적용한 직후에서 1 개월 경과된 후까지 유의하게 지각과민증을 완화시키는 것이 관찰되었다고 하였다. Bifluorid 12는 적용한 직후에는 열 자극과 기계적 자극 민감성에 대한 완화효과를 보였으나, 1 개월 경과한 후에는 기계적 자극에 대한 민감성 완화효과를 보이지 않았다고 하였다. Pesevska 등 (2010)은 스케일링 또는 치근 활택술 후에 발생하는 상아질 지각과민증을 완화시키기 위하여 저강도 레이저 치료와 국소불소제재를 도포하여 2 일과 4 일 경과한 다음 완화된 효과를 비교한 결과 레이저 치료한 경우에는 86.6%에서 완전히 통증이 소멸된 반면, 국소불소제재를 도포한 경우에는 26.6%에서만 소멸된 것이 관찰되었다고 하였다. Rusin 등 (2010)은 본 연구와 유사한 흐름율 측정장치를 이용한 연구에서 레진강화형 글라스아이오노머 시멘트 또는 상아질 접착제가 노출된 치근부 상아질의 민감성 완화에 효과적이라고 하였다. 그러나 Strober 등 (2013)은 중간 깊이의 1 급 및 2 급 와동 수복물의 경우 레진 강화형 글라스아이오노머 이장재의 지각과민증 완화 효과는 관찰되지 않았다고 하였다.
Kolker 등 (2002)은 Seal & Protect, Gluma Desensitizer, HurriSeal, D/Sense 2 및 Super Seal 등이 상아질 투과도와 상아세관 봉쇄능에 주는 영향을 평가하였는데, 상아질 투과도와 SEM 관찰 결과는 명확한 상관성을 보이지 못하였으며, Super Seal의 투과도 감소 효과가 가장 우수하였다고 발표하였다. 반면, 본 연구에서는 흐름율로 평가한 상아질 투과도와 SEM 관찰로 평가한 상아세관 봉쇄 정도에서 상관성이 관찰되었다.
Ⅴ. CONCLUSION
본 연구 결과 비우식성 치경부 병소가 있는 치아를 스케일링 처리하는 과정에서 상아세관이 노출되어 지각과민증이 유발된 경우에는 기능성 레진이 함유된 지각과민처치제 적용이 가장 우수한 효과를 보여 지각과민증 치료를 위한 적절한 지각과민처치제로 제안될 수 있으며, 다른 지각과민처치제를 적용하는 경우 상아질 접착제를 추가로 적용하는 방법을 제시할 수 있다. 또한 건전한 치아의 경우 통상적인 초음파 스케일링에 의한 상아질 노출 가능성은 크지 않은 것으로 보여 치석 제거 등을 위한 초음파 스케일링에는 문제가 없는 것으로 보이지만, 치경부 병소가 있는 부위는 초음파 스켈링시 치질 삭제로 인한 상아세관 노출에 세심한 주의가 필요할 것으로 보인다.
Acknowledgments
이 논문은 2013년도 정부( 교육부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구사업임 (No. NRF-2013R1A1A2005410).
References
- 신혜련, 이만섭, 권영혁, (1988), 치주 수술 후 노출된 치근에서 발생하는 지각 과민증의 발생 양태에 관한 연구, 대한치주과학회지, 18, p174-185.
- 조재형, 김기동, 석수황, 임범순, (2014), 다양한 성분의 지각과민처치제가 4세대 상아질 접착제의 접착력에 주는 영향, 대한치과재료학회지, 41, p81-290.
-
Addy, M., Pearce, N., (1994), Aetilolgical, predisposing and environmental factors in dentin hypersensitivity, Arch Oral Biol, 39(Suppl), pS33-S38.
[https://doi.org/10.1016/0003-9969(94)90186-4]

-
Aranha, AC., Pimenta, LA., Marchi, GM., (2009), Clinical evaluation of desensiti- zing treatments for cervical dentin hypersensitivity, Braz Oral Res, 23, p333-339.
[https://doi.org/10.1590/S1806-83242009000300018]

- Bamise, CT., Esan, TA., (2011), Mechanisms and treatment approaches of dentine hypersensitivity: a literature review, Oral Health Prev Dent, 9, p353-367.
-
Barrientos, C., Xaus, G., Leighton, C., Martin, J., Gordan, VV., Moncada, G., (2011), Oxalic acid under adhesive restorations as a means to reduce dentin sensitivity: a four-month clinical trial, Oper Dent, 36, p126-132.
[https://doi.org/10.2341/09-364-C]

-
Bartlett, DW., Shah, P., (2006), A critical review of non-carious cervical (wear) lesions and the role of abfraction, erosion, and abrasion, J Dent Res, 85, p306-312.
[https://doi.org/10.1177/154405910608500405]

-
Boksman, LL., Swift, EJ. Jr, (2011), Critical appraisal. Current usage of glutaraldehyde/HEMA, J Esthet Restor Dent, 23, p410-416.
[https://doi.org/10.1111/j.1708-8240.2011.00490.x]

-
Bräxnnströym, M., Lindéxn, LA., Aströym, A., (1967), The hydrodynamics of the dental tubule and of pulp fluid. A discussion of its significance in relation to dentinal sensitivity, Caries Res, 1, p310-317.
[https://doi.org/10.1159/000259530]

- Camps, J., About, I., Van Meerbeek, B., Franquin, JC., (2002), Efficiency and cytotoxicity of resin-based desensitizing agents, Am J Dent, 15, p300-304.
- Chabanski, MB., Gillam, DG., Bulman, JS., Newman, HN., (1997), Clinical evaluation of cervical dentine sensitivity in a population of patients referred to a specialist periodontology department: a pilot study, J Oral Rehabil, 24(9), p666-672.
-
Cunha-Cruz, J., Stout, JR., Heaton, LJ., Wataha, JC., Northwest PRECEDENT, (2011), Dentin hypersensitivity and oxalates: a systematic review, J Dent Res, 90, p304-310.
[https://doi.org/10.1177/0022034510389179]

- de Andrade e Silva, SM., Marquezini, L. Jr, Manso, AP., Garcia, FP., Carrilho, MR., Pashley, DH., Tay, FR., Carvalho, RM., (2007), Effects of a combined application of potassium oxalate gel/adhesive agent on dentin permeability in vitro, J Adhes Dent, 9, p505-512.
- de Assis Cde, A., Antoniazzi, RP., Zanatta, FB., Röxsing, CK., (2006), Efficacy of Gluma Desensitizer on dentin hypersensitivity in periodontally treated patients, Braz Oral Res, 20, p252-256.
- Dijkman, GE., Jongebloed, WL., de Vries, J., Ogaard, B., Arends, J., (1994), Closing of dentinal tubules by glutardaldehyde treatment, a scanning electron microscopy study, Scand J Dent Res, 102, p144-150.
- Felton, DA., Bergenholz, G., Kanoy, BE., (1991), Evaluation of the desensitizing effect of Gluma Dentin Bond on teeth prepared for complete- coverage restorations, Int J Prostodont, 4, p292-298.
-
Fu, B., Shen, Y., Wang, H., Hannig, M., (2007), Sealing ability of dentin adhesives/desensitizer, Oper Dent, 32, p496-503.
[https://doi.org/10.2341/06-143]

-
Grippo, JO., (1992), Noncarious cervical lesions: the decision to ignore or restore, J Esthet Dent, 4(Suppl), p55-64.
[https://doi.org/10.1111/j.1708-8240.1992.tb00721.x]

-
Haugen, E., Johansen, JR., (1988), Tooth hypersensitivity after periodontal treatment. A case report including SEM studies, J Clin Periodontol, 15, p399-401.
[https://doi.org/10.1111/j.1600-051X.1988.tb01018.x]

-
Hoang-Dao, BT., Hoang-Tu, H., Tran-Hung, L., Camps, J., Koubi, G., About, I., (2008), Evaluation of a natural resin-based new material (Shellac F) as a potential desensitizing agent, Dent Mater, 24, p1001-1007.
[https://doi.org/10.1016/j.dental.2007.11.014]

-
Ishihata, H., Kanehira, M., Finger, WJ., Shimauchi, H., Komatsu, M., (2012), Effects of applying glutaraldehyde-containing desensitizer formulations on reducing dentin permeability, J Dent Sci, 7, p105-110.
[https://doi.org/10.1016/j.jds.2012.03.005]

- Jacobsen, PL., Bruce, G., (2001), Clinical dentin hypersensitivity: understanding the causes and prescribing a treatment, J Contemp Dent Pract, 2, p1-12.
- Kakaboura, A., Rahiotis, C., Thomaidis, S., Doukoudakis, S., (2005), Clinical effectiveness of two agents on the treatment of tooth cervical hypersensitivity, Am J Dent, 18, p291-295.
-
Kim, SY., Ferracane, J., Kim, HY., Lee, IB., (2010), Realtime measurement of dentinal fluid flow during amalgam and composite restoration, J Dent, 38, p343-351.
[https://doi.org/10.1016/j.jdent.2009.12.008]

-
Kim, SY., Kim, EJ., Kim, DS., Lee, IB., (2013), The evaluation of dentinal tubule occlusion by desensitizing agents: a real-time measurement of dentinal fluid flow rate and scanning electron microscopy, Oper Dent, 38, p419-428.
[https://doi.org/10.2341/11-504-L]

- Kolker, JL., Vargas, MA., Armstrong, SR., Dawson, DV., (2002), Effect of desensitizing agents on dentin permeability and dentin tubule occlusion, J Adhes Dent, 4, p211-221.
-
Komabayashi, T., Imai, Y., Ahn, C., Chow, LC., Takagi, S., (2010), Dentin permeability reduction by a sequential application of calcium and fluoride-phosphate solutions, J Dent, 38, p736-741.
[https://doi.org/10.1016/j.jdent.2010.05.019]

- Larson, TD., (2013), Clinical uses of glutaraldehyde/2-hydroxyethylmethacrylate (GLUMA), Northwest Dent, 92, p27-30.
-
Lee, WC., Eakle, WS., (1996), Stress-induced cervical lesions: review of advances in the past 10 years, J Prosthet Dent, 75, p487-494.
[https://doi.org/10.1016/S0022-3913(96)90451-5]

-
Mantzourani, M., Sharma, D., (2013), Dentine sensitivity: past, present and future, J Dent, 41, pS3-S17.
[https://doi.org/10.1016/S0300-5712(13)70002-2]

-
Mitchell, JC., Musanje, L., Ferracane, JL., (20110), Biomimetic dentin desensitizer based on nano-structured bioactive glass, Dent Mater, 27, p386-393.
[https://doi.org/10.1016/j.dental.2010.11.019]

-
Orchardson, R., Gillam, DG., (2006), Managing dentin hypersensitivity, J Am Dent Assoc, 137, p990-998.
[https://doi.org/10.14219/jada.archive.2006.0321]

-
Pamir, T., Dalgar, H., Onal, B., (2007), Clinical evaluation of three desensitizing agents in relieving dentin hypersensitivity, Oper Dent, 32, p544-548.
[https://doi.org/10.2341/07-5]

-
Pashley, DH., (1986), Dentin permeability, dentin sensitivity, and treatment through tubule occlusion, J Endod, 12, p465-474.
[https://doi.org/10.1016/S0099-2399(86)80201-1]

- Pashley, DH., (1984), Smear layer: Physiological considerations, Oper Dent, 3(suppl), p13-29.
-
Pashley, DH., Galloway, SE., (1985), The effects of oxalate treatment on the smear layer of ground surfaces of human dentine, Arch Oral Biol, 30, p731-737.
[https://doi.org/10.1016/0003-9969(85)90185-2]

- Pashley, DH., Carvalho, RM., Pereira, JC., Villanueva, R., Tay, FR., (2001), The use of oxalate to reduce dentin permeability under adhesive restorations, Am J Dent, 14, p89-94.
- Patel, R., Chopra, S., Vandeven, M., Cummins, D., (2011), Comparison of the effects on dentin permeability of two commercially available sensitivity relief dentifrices, J Clin Dent, 22, p108-112.
-
Pesevska, S., Nakova, M., Ivanovski, K., Angelov, N., Kesic, L., Obradovic, R., Mindova, S., Nares, S., (2010), Dentinal hypersensitivity following scaling and root planing: comparison of low-level laser and topical fluoride treatment, Lasers Med Sci, 25, p647-650.
[https://doi.org/10.1007/s10103-009-0685-0]

-
Pillon, FL., Romani, IG., Schmidt, ER., (2004), Effect of a 3% potassium oxalate topical application on dentinal hypersensitivity after subgingival scaling and root planing, J Periodontol, 75, p1461-1464.
[https://doi.org/10.1902/jop.2004.75.11.1461]

-
Piotrowski, BT., Gillette, WB., Hancock, EB., (2001), Examining the prevalence and characteristics of abfractionlike cervical lesions in a population of U.S. veterans, J Am Dent Assoc, 132, p1694-1701.
[https://doi.org/10.14219/jada.archive.2001.0122]

-
Que, K., Guo, B., Jia, Z., Chen, Z., Yang, J., Gao, P., (2013), A cross-sectional study: non-carious cervical lesions, cervical dentine hypersensitivity and related risk factors, J Oral Rehabil, 40, p24-32.
[https://doi.org/10.1111/j.1365-2842.2012.02342.x]

-
Que, K., Ruan, J., Fan, X., Liang, X., Hu, D., (2011), A multi-centre and crosssectional study of dentine hypersensitivity in China, J Clin Periodontol, 37, p631-637.
[https://doi.org/10.1111/j.1600-051X.2009.01513.x]

-
Ritter, AV., Heyamann, HO., Swift, EJ. Jr, Perdigäyo, J., Rosa, BT., (2000), Effects of different re-wetting techniques on dentin shear bond strengths, J Esthet Dent, 12, p85-96.
[https://doi.org/10.1111/j.1708-8240.2000.tb00205.x]

-
Ritter, AV., de L Dias, W., Miguez, P., Caplan, DJ., Swift, EJ. Jr, (2006), Treating cervical dentin hypersensitivity with fluoride varnish: a randomized clinical study, J Am Dent Assoc, 137, p1013-1020.
[https://doi.org/10.14219/jada.archive.2006.0324]

-
Rusin, RP., Agee, K., Suchko, M., Pashley, DH., (2010), Effect of a new desensitizing material on human dentin permeability, Dent Mater, 26, p600-607.
[https://doi.org/10.1016/j.dental.2010.02.010]

-
Santiago, SL., Pereira, JC., Martineli, AC., (2006), Effect of commercially available and experimental potassium oxalate-based dentin desensitizing agents in dentin permeability: influence of time and filtration system, Braz Dent J, 17, p300-305.
[https://doi.org/10.1590/S0103-64402006000400007]

-
Schüxpbach, P., Lutz, F., Finger, WJ., (1997), Closing of dentinal tubules by Gluma desensitizer, Eur J Oral Sci, 105, p414-421.
[https://doi.org/10.1111/j.1600-0722.1997.tb02138.x]

-
Strober, B., Veitz-Keenan, A., Barna, JA., Matthews, AG., Vena, D., Craig, RG., Curro, FA., Thompson, VP., (2013), Effectiveness of a resin-modified glass ionomer liner in reducing hypersensitivity in posterior restorations: a study from the practitioners engaged in applied research and learning network, J Am Dent Assoc, 144, p886-897.
[https://doi.org/10.14219/jada.archive.2013.0206]

- Terry, DA., (2011), Cervical dentin hypersensitivity: Etiology, diagnosis, and management, Dent Today, 30, p61-68.
- Udoye, CI., (2006), Pattern and distribution of cervical dentine hypersensitivity in a Nigerian tertiary hospital, Odontostomatol Trop, 29, p19-22.
-
Vieira, AH., Passos, VF., de Assis, JS., Mendonçya, JS., Santiago, SL., (2009), Clinical evaluation of a 3% potassium oxalate gel and a GaAlAs laser for the treatment of dentinal hypersensitivity, Photomed Laser Surg, 27, p807-812.
[https://doi.org/10.1089/pho.2008.2364]

- Walters, PA., (2005), Dentinal hypersensitivity: a review, J Contemp Dent Pract, 6, p107-117.
-
West, NX., (2008), Dentine hypersensitivity: preventive and therapeutic approaches to treatment, Periodontol 2000, 48, p31-41.
[https://doi.org/10.1111/j.1600-0757.2008.00262.x]

-
Wolff, MS., (2009), Dentin hypersensitivity, the biofilm and remineralization: what is the connection?, Adv Dent Res, 21, p21-24.
[https://doi.org/10.1177/0895937409335618]

-
Yoshiyama, M., Masada, J., Uchida, A., Ishida, H., (1989), Scanning electron microscopic characterization of sensitive vs. insensitive human radicular dentin, J Dent Res, 68, p1498-1502.
[https://doi.org/10.1177/00220345890680110601]

-
Yu, X., Liang, B., Jin, X., Fu, B., Hannig, M., (2010), Comparative in vivo study on the desensitizing efficacy of dentin desensitizers and one-bottle self-etching adhesives, Oper Dent, 35, p279-286.
[https://doi.org/10.2341/09-346-C]