
구강 상처 치유를 위한 합성 고분자 기반 생체재료의 응용
초록
구강 상처는 복잡한 해부학적 구조, 지속적인 기계적 자극, 미생물이 풍부한 습윤 환경 등의 특수한 조건으로 인해 치유 과정이 까다롭다. 기존의 봉합이나 거즈 등 전통적인 처치 방식은 구강 내에서의 기능적 요구를 충족시키기 어려우며, 이로 인해 보다 진보된 상처 관리 전략이 요구되고 있다. 합성 고분자는 조절 가능한 물리화학적 특성을 바탕으로 구강 상처 드레싱 소재로 주목받고 있으며, 점착성 부여, 약물 방출 조절, 항균 작용, 조직 재생 유도 등의 기능을 수행할 수 있다. 본 리뷰에서는 구강 상처 환경의 특성과 고분자 드레싱 설계에 필요한 핵심 고려 요소를 정리하고, 주요 합성 고분자의 구조적 특성, 생물학적 기능, 임상 적용 가능성을 중심으로 고찰하였다. 또한, 약물 전달, 항균 효과, 조직 재생 촉진을 위한 기능적 전략과 그에 대한 전임상 및 임상 사례도 함께 논의하였다. 본 리뷰는 고분자 소재 과학과 임상 요구사항을 통합적으로 연결함으로써, 구강 상처 치료를 위한 차세대 합성 고분자 드레싱의 개발 방향과 임상 적용 가능성을 제시하고자 한다.
Abstract
Oral wound healing poses unique challenges due to the anatomical complexity, continuous mechanical irritation, and moist environment rich in microorganisms. Conventional treatments such as sutures and gauze are often inadequate in meeting the specific functional demands of the oral cavity, necessitating more advanced therapeutic approaches. Synthetic polymers have emerged as promising materials for oral wound dressings owing to their tunable physicochemical properties, which allow for functions such as wet adhesion, controlled drug release, antimicrobial activity, and tissue regeneration. This review comprehensively summarizes the characteristics of the oral wound environment and outlines key design criteria for effective polymeric dressings. It focuses on the structural features, biological functions, and clinical relevance of major synthetic polymers widely utilized in clinical or preclinical settings. Strategies to enhance drug delivery, antimicrobial efficacy, and tissue regeneration are also discussed. Furthermore, commercial products and relevant preclinical/clinical studies are presented to highlight the translational potential of polymer-based systems. By systematically integrating material science with clinical needs, this review aims to guide the development of next-generation multifunctional synthetic polymer dressings for oral wound care.
Keywords:
Oral wound, Healing, Tissue adhesive, Synthetic polymer, Biomaterial키워드:
구강 상처, 치유, 조직접착제, 합성 고분자, 생체재료서 론
구강은 음식 섭취, 발화, 감각 인지 등 다양한 생체 기능을 수행하는 복합적인 해부학적 구조를 가진 기관이다. 구조적으로 복잡한 구강은 점막, 근육, 침샘, 치아, 그리고 치조골로 구성되어 있으며, 이들 모두는 외부 환경으로부터의 물리적 및 화학적 자극에 지속적으로 노출되어 있다. 구강 내 상처는 점막의 단순 손상부터 외과적 절개, 감염성 궤양, 외상성 열상에 이르기까지 다양하며, 치유 과정은 복잡한 환경적 요인의 영향을 받아 피부보다 훨씬 복잡하다(1, 2).
특히 구강은 항상 습윤한 상태로 유지되며, 다양한 세균과 효소가 존재하는 특수한 미생물 환경을 지닌다. 또한 말하기, 씹기, 삼키기 등 반복적인 움직임으로 인해 상처 부위가 지속적으로 자극을 받게 되며, 이로 인해 상처의 재손상과 감염 위험이 증가하고, 치유가 지연되며 통증, 출혈, 연하 곤란, 심리적 불편감을 유발하여 삶의 질을 저하시킨다(3-5). 따라서 구강 내 상처는 단순한 물리적 봉합이나 일반적인 상처 보호로는 효과적인 치료가 어려운 특수한 영역이다.
기존에는 봉합, 거즈나 거치형 드레싱, 자가 조직 이식 등이 주된 치료 방식으로 활용되어 왔지만, 이는 고정이 어렵고 감염 방지 효과가 제한적이며, 교체 시 추가적인 손상이나 환자의 불편함을 유발하는 단점이 있다(6-8). 특히 조직 이식의 경우 공여 부위 손상이나 면역 반응 유발 등의 부담이 존재한다. 따라서 구강 환경에 보다 적합하고 생체 친화적이며 기능적으로 향상된 드레싱 소재의 개발이 요구된다.
이러한 배경에서 최근 주목받고 있는 것이 바로 합성 고분자 기반의 기능성 드레싱이다. 합성 고분자는 물리적 특성과 생분해성을 조절하기 용이하며, 약물 전달, 항균성, 점막 부착력, 조직 재생 유도 등 다양한 기능을 부여할 수 있는 높은 설계 유연성을 제공한다(9). 특히 구강 내 복잡한 환경에 대응하기 위해 자극 반응성(pH 또는 온도), 습윤 접착력 강화, 약물 방출 속도 조절 등 맞춤형 기능 구현이 가능한 점에서 천연 고분자보다 더 높은 활용 가능성을 보여주고 있다(10-12).
본 리뷰는 구강 내 상처 치유에 있어서 합성 고분자 드레싱 소재의 가능성과 실제 응용 사례를 종합적으로 고찰하는 것을 목적으로 한다. 구강 환경의 특수성을 기반으로 한 합성시의 고려사항, 대표적인 합성 고분자의 종류 및 특성, 기능성 부여 전략, 상용 제품과 전임상 및 임상 연구 현황 등을 중심으로 논의하여 향후 구강 조직 재생 및 드레싱 소재 개발에 있어 보다 효과적인 접근 방향과 연구 전략 수립에 기여하고자 한다. 구강 상처 치유의 복합적인 장벽 요소들과 이를 해결하기 위한 합성 고분자 드레싱의 주요 기능적 역할은 Figure 1에 도식적으로 요약하였다. 이 도식은 구강 환경의 생물학적/역학적 특성과 드레싱이 수행해야 할 핵심 기능을 직관적으로 이해할 수 있도록 구성되었다.
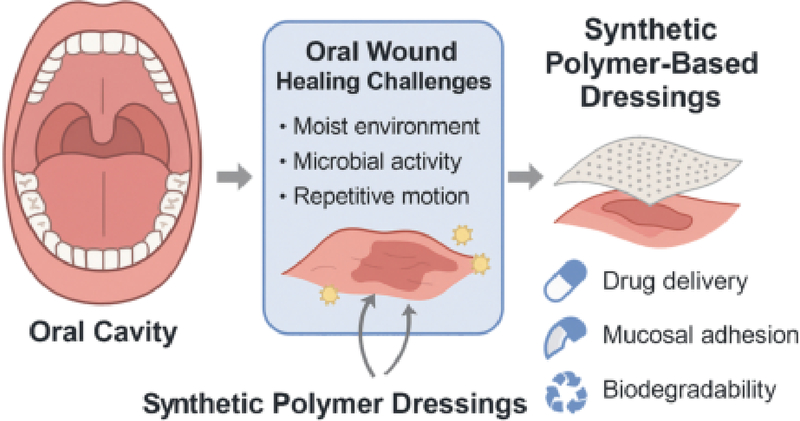
Schematic illustration summarizing the major challenges of oral wound healing and the corresponding functional roles of synthetic polymer-based dressings. The diagram highlights biological and mechanical barriers specific to the oral environment and outlines strategies by which advanced polymeric dressings can overcome these obstacles.
본 론
1. 구강 내 환경에 최적화된 합성 고분자 드레싱 개발의 고려사항
구강 내 환경은 피부나 일반적인 외부 상처 부위와는 본질적으로 매우 다르다. 구강은 지속적인 타액 분비로 인해 항상 습윤 상태이며, 섭식, 호흡 등에 따라 온도와 pH가 빈번하게 변동한다(13, 14). 또한 수백 종 이상의 미생물이 밀집된 고밀도 미생물 군집 환경이며, 말하기, 씹기, 삼키기와 같은 지속적인 기계적 움직임으로 인해 상처 부위가 끊임없이 자극받는다(15, 16). 이러한 복합적인 생물학적 그리고 역학적인 특성은 드레싱 재료가 고정되기 어렵고 기능을 안정적으로 유지하기 힘든 조건을 형성한다.
구강 내 드레싱의 가장 주요한 점은 습윤 환경에서도 안정적인 접착력을 유지할 수 있어야 한다는 것이다. 일반 피부용 드레싱은 건조한 표면을 전제로 준비되어 있어, 타액이 존재하는 구강에서는 부착력이 크게 저하된다. 이에 따라 습윤 접착성을 강화한 특성이 필수적이며, 합성 고분자에서는 카테콜기 등의 화학적 작용기를 도입하거나, 미세구조 기반의 물리적 결합 방식을 적용함으로써 구현할 수 있다(17-19). 이는 드레싱이 점막에 자극 없이 부착되어 장시간 안정성을 유지하는 데 기여한다.
또 하나의 중요한 특성은 미생물 감염과 바이오필름 형성에 대한 저항성이다. 구강 내 상처는 다양한 균종에 노출되어 있으며, 특히 Streptococcus mutans나 Porphyromonas gingivalis와 같은 병원성 세균은 염증 반응을 유발하고 조직 재생을 저해할 수 있다. 이로 인해 드레싱 표면이 오히려 세균 번식의 매개체가 될 위험도 존재한다(13, 14). 이에 따라 합성 고분자 기반 드레싱에는 항균 물질을 포함하거나, pH 반응성 또는 효소 반응성 방출 시스템을 도입하여 감염 예방을 도모하는 개발이 시도되고 있다(20, 21). 또한 표면의 소수성 및 친수성을 조절하거나 전하를 부여하는 등 세균 부착 자체를 억제하는 방법도 병행되고 있다(22, 23).
기계적 물성과 내구성 역시 구강 드레싱에서 중요한 성능이다. 구강 내 상처는 지속적인 압력, 마찰, 신장력에 노출되기 때문에 드레싱은 탄성, 유연성, 인장강도를 고루 갖추어야 하며, 동시에 상처 부위에 자극을 주지 않아야 한다(24-26). Polyurethane (PU) 및 polycaprolactone (PCL)과 같은 합성 고분자는 이러한 물성을 조절하기 용이하며, 필름, 하이드로겔, 나노섬유 등 다양한 형태로 가공 가능하다(27-29).
또한 구강 내 드레싱은 생분해성과 생체적합성 측면에서도 적합한 안전성을 요구한다. 일부 드레싱은 제거되지 않고 체내에서 흡수되거나 우연히 삼켜질 수 있으므로, 독성이 없고 염증 반응을 유발하지 않는 분해산물을 형성해야 한다(3, 30). Poly(lactic-co-glycolic acid) (PLGA) 및 polyethylene glycol (PEG)은 이러한 조건을 만족시키며 미국식품의약국(Food and Drug Administration, FDA) 승인도 받은 재료로 널리 사용된다(31, 32). 특히, 드레싱의 분해 속도를 치유 주기와 조화롭게 디자인하는 것이 중요하다(33, 34).
마지막으로, 임상 적용의 편의성과 임상 사용자 중심의 디자인도 실용적 관점에서 중요하다. 드레싱은 복잡한 기구 없이 간편하게 적용 가능해야 하며, 환자의 일상생활에 불편을 초래하지 않아야 한다. 주사형 하이드로겔이나 스프레이형 필름은 불규칙한 구강 상처에도 잘 적응되며(35, 36), 열 또는 pH 반응을 통해 치유 환경에 따라 약물 방출을 자동으로 조절하는 스마트 드레싱 시스템 개발도 활발히 이루어지고 있다(37, 38).
요약하자면, 구강 내 상처 치료에 적합한 합성 고분자 드레싱을 설계하기 위해서는 구강의 복잡한 환경 조건을 충분히 고려하고, 재료의 접착성, 항균성, 기계적 특성, 분해 거동, 임상 편의성을 종합적으로 조율해야 한다. 이러한 정교한 설계를 통해 합성 고분자 기반 드레싱은 기존 치료법의 한계를 보완하고, 구강 조직의 효과적인 재생을 유도하는 차세대 치료 전략으로 발전할 수 있다. 이러한 설계 고려 요소들을 시각적으로 정리한 개요는 Figure 2에 제시되어 있으며, 구강 내 적용을 위한 주요 기능 요건을 개괄적으로 보여준다.
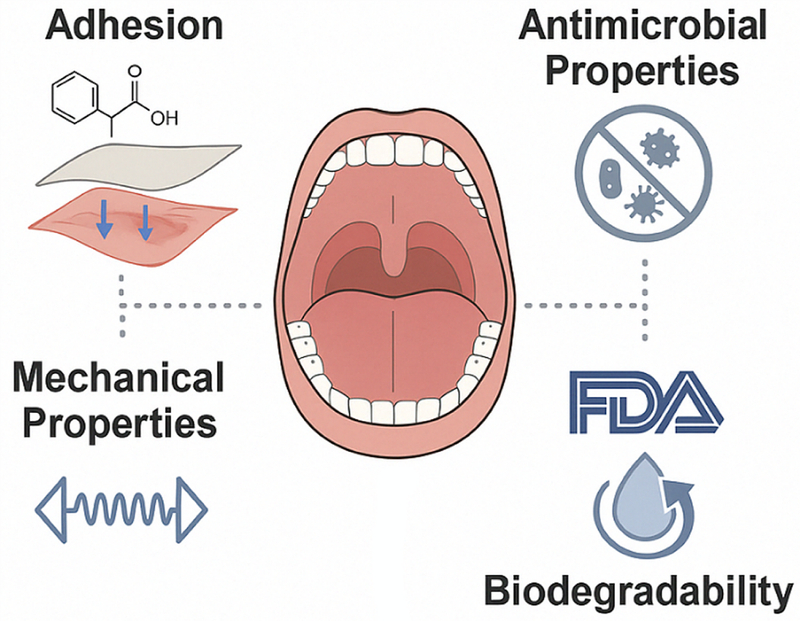
Key considerations in the design of synthetic polymer-based dressings optimized for intraoral application. The illustration outlines the essential material characteristics - such as wet adhesion, antimicrobial activity, mechanical stability, biodegradability, and clinical usability - required to function effectively within the unique oral environment.
2. 구강 상처 치료에 적용되는 주요 합성 고분자
합성 고분자는 분자 구조를 정밀하게 조절할 수 있으며, 생체적합성, 기계적 강도, 분해 속도, 표면 특성 등 다양한 물성을 필요에 따라 설계할 수 있다는 점에서 구강 내 상처 치료에 매우 유리한 재료이다(9). 구강이라는 특수한 생물학적 및 기계적 환경에서 요구되는 다기능성, 예를 들어, 습윤 접착력, 약물 전달 능력, 항균성, 생분해성, 조직 재생 유도력 등을 구현하기 위해서 소재의 미세 조정이 가능한 합성 고분자의 특징은 매우 적합하다고 할 수 있다(39). 본 절에서는 구강 내 드레싱에 널리 연구되었거나 적용된 주요 합성 고분자들을 생분해성 고분자와 비분해성 고분자로 나누어 설명하고, 이들의 구조적 특성과 치료적 장점을 소개하고자 한다.
Polyvinyl alcohol (PVA)는 대표적인 수용성 고분자로, 생체적합성이 우수하여 의료용 드레싱 소재로 널리 사용된다(40). PVA는 화학적 혹은 물리적 가교를 통해 하이드로겔 형태로 제조할 수 있으며, 점막 표면에 부드럽게 부착되고 수분을 유지하는 기능이 탁월하다(41). 이는 구강 내에서 얇고 유연한 보호막을 형성할 수 있어, 상처 부위의 기계적 자극을 완화하고, 첨가한 항균제 또는 항염제의 치유 효과를 극대화할 수 있다(42). 또한 PVA는 전기방사법으로 나노섬유화가 가능하여, 세포 유도 지지체로도 활용될 수 있다(43).
Polyethylene glycol (PEG)은 친수성 및 생체적합성이 매우 뛰어난 고분자로, 약물 전달 시스템이나 생분해성 하이드로겔의 구성 요소로 자주 활용된다(44). 다양한 분자량 범위에서 사용 가능하며, 다른 고분자와의 블렌딩이나 공중합체 형성이 쉬워 다기능 복합 시스템 구축에 용이하다(45). 특히 pH 변화, 효소 환경, 온도 반응성 등의 특성을 설계에 반영할 수 있어, 자극 반응성 드레싱 개발에 적합하다(44). PEG 기반 드레싱은 예측 가능한 분해 거동과 약물 방출 속도 조절이 가능하여, 장기적인 구강 상처 관리에도 유효하다(46).
Poly(lactic-co-glycolic acid) (PLGA)는 체내에서 젖산과 글리콜산으로 분해되며 독성이 없어 FDA 승인을 받은 생분해성 고분자이다. 분해 속도 조절이 가능하고, 나노입자, 마이크로스피어, 하이드로겔 등 다양한 형태로 가공할 수 있어, 지속 방출형 약물전달체로 많이 활용된다(47, 48). 구강 상처 부위에 적용 시, PLGA에 성장인자나 항생제를 탑재함으로써 염증 억제와 조직 재생을 동시에 유도할 수 있으며, 특히 연조직 결손 부위나 골막 부위 등에서 효과적으로 작용하는 것으로 보고되고 있다(49).
Polycaprolactone (PCL)은 PLGA에 비해 분해 속도가 느린 고분자이지만, 조직 재생을 위한 지지체로서 많이 연구되고 있다(50). 낮은 융점과 우수한 가공성으로 인해 전기방사 기반 나노섬유 패치 제작에 적합하며, 구강 점막의 복잡한 구조에도 효과적으로 적용될 수 있다(51). 따라서 성장인자나 세포를 함께 로딩하여 조직공학적 드레싱으로 응용할 수 있고, 구개 결손 등 장기적인 재건이 필요한 부위에 적합한 것으로 알려져 있다(52).
Polyurethane (PU)은 높은 인장강도와 유연성을 동시에 갖춘 비분해성 고분자로, 구강 내 반복적인 기계적 자극에도 잘 견딜 수 있는 재료이다(53). 필름, 폼, 나노섬유 등 다양한 형태로 가공할 수 있으며, 통기성과 내수성이 뛰어나 드레싱의 안정적인 유지에 유리하다(54). 최근에는 전기방사법을 통해 나노섬유 형태의 지지체를 제작하여 상피세포 부착 및 증식을 유도하는 연구도 진행되고 있으며, 이는 상처 회복을 넘어 조직 재건의 가능성까지 제시한다(55).
Polytetrafluoroethylene (PTFE) 또한 구강 상처 치료에서 널리 활용되는 대표적인 비분해성 합성 고분자이다. PTFE는 생체적합성이 매우 우수하고 화학적 안정성이 뛰어나며, 조직 내 삽입 시 염증 반응을 최소화하는 특성이 있다. 특히 non-resorbable membrane 형태로 제작되어 치주조직 재생술(GTR; guided tissue regeneration)이나 구강 점막 재건에 자주 사용된다. PTFE는 세균 부착을 억제하는 표면 특성을 지녀 감염 예방에 효과적이며, 미세기공 구조 여부에 따라 고정성과 조직 반응성이 달라질 수 있다. 최근에는 e-PTFE (expanded PTFE) 및 d-PTFE (dense PTFE)를 포함한 다양한 형태의 PTFE 멤브레인이 임상에서 활용되고 있으며, 특히 치조골 보존 및 유도 조직 재생 분야에서 그 효과가 입증되고 있다(56, 57).
기능성 고분자인 pH 감응성 고분자(polyacrylic acid, PAA), 온도 감응성 고분자(poly(N-isopropylacrylamide, PNIPAM), 전기전도성 고분자(poly(3,4-ethylenedioxythiophene), PEDOT) 등은 생분해성 여부보다는 자극 반응성, 전기전도성, 환경 적응성 등 스마트 기능 구현에 초점이 맞춰진 재료이다(58-60). 단독 혹은 복합재 형태로 설계되어 약물 전달이나 항균 코팅 등에 활용되며, 향후 구강 환경에 적응하는 스마트 드레싱 개발에 핵심적인 역할을 할 수 있다.
위에서 소개한 주요 합성 고분자들의 구조적 특성, 대표적인 드레싱 형태, 기능적 장점, 그리고 구강 내 적용상의 이점을 요약한 내용은 Table 1에 정리되어 있다. Table 1에 제시된 고분자들 중 일부(PVA, PEG, 및 PLGA)는 특정 약물 전달 시스템이나 의료기기 등에 사용되어 FDA의 승인을 받은 사례가 있으나, 이는 각각의 제형 및 적용 목적에 따라 달라질 수 있다.
3. 합성 고분자의 기능성 응용과 실제 적용
합성 고분자 기반 드레싱은 단순한 물리적 보호를 넘어, 상처 치유에 실질적으로 기여할 수 있는 다양한 기능을 수반하는 역할을 수행할 수 있다. 약물 전달, 항균 효과, 조직 재생 유도는 구강 상처 치유를 위한 핵심 전략으로 최근에는 이를 전임상 및 임상 단계까지 확장하는 연구도 활발히 이루어지고 있다.
합성 고분자는 약물 전달체로서 아주 적합한 소재이다. PVA, PEG, PLGA, PU 등 다양한 고분자는 항생제, 항염증제, 진통제, 성장인자(EGF, VEGF 등)를 로딩하여 국소 지속 방출 시스템을 구축할 수 있다(39, 49). 특히 pH 변화나 온도 등의 환경 자극에 따라 약물 방출을 조절하는 스마트 드레싱으로의 응용도 활발히 연구되고 있으며, 이는 감염 위험이 높은 구강 상처에 매우 유용할 것이다(58).
항균성과 항염 효과는 구강 상처 드레싱에서 필수적인 요소다 합성 고분자에 은 나노입자, 산화아연, 클로르헥시딘 등의 항균 물질을 탑재하거나, 고분자 자체에 항균 기능을 도입하는 방식으로 미생물 정착 및 바이오필름 형성 억제가 가능하다(20, 42, 61). 예를 들어, 표면에 정전기적 특성을 부여하거나 친수성/소수성을 조절하여 세균 부착을 억제하는 기술도 적용되고 있다(62).
또한, 일부 고분자 드레싱은 조직 재생 촉진 기능도 갖추고 있다. 전기방사법으로 제조된 PCL 기반 나노섬유는 세포 부착과 증식을 유도하는 구조적 scaffold로 작용하며, 일부 연구에서는 골막, 구개 점막 등의 재건에도 적용 가능성이 확인되었다(51, 63). 특히 성장인자를 탑재한 다층 구조의 드레싱은 상피세포화를 촉진하고 염증 반응을 억제하는 데 효과적이다(64).
이러한 기술들은 점차 상용 제품과 전임상/임상 연구로도 연결되고 있다. 예를 들어, Ora-Aid®는 자가 접착성이 있는 구강 드레싱으로, 소형 수술 후 상처 보호에 사용되며 환자 만족도가 높다(65). OraSoothe® Sockit Gel은 PEG 기반 드레싱으로, 항염증 및 진통 효과를 갖추고 있으며 상용 제품으로 활용되고 있다(66). 최근에는 성장인자 탑재 PLGA 하이드로겔을 적용한 동물실험에서 조직 재생 가속 및 감염 억제 효과가 입증되기도 했다(67). 이러한 기능성 드레싱의 항균 효과, 약물 방출, 조직 재생 유도 능력은 Figure 3에 제시된 전임상 사례들을 통해 입증되고 있다.
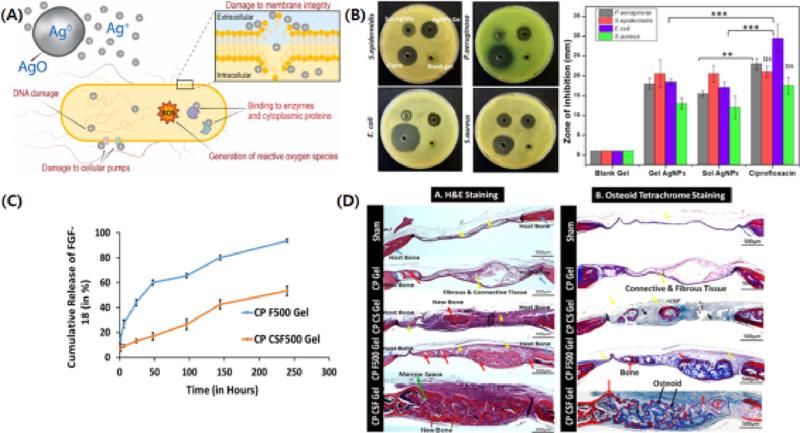
(A) Proposed antibacterial mechanisms of silver nanoparticles incorporated into polymeric materials. Reprinted with permission from (20). Copyright 2024 Elsevier. (B) Antibacterial effects of a silver nanoparticle-loaded disk against S. epidermidis, P. aeruginosa, E. coli, and S. aureus, with quantitative analysis of inhibition zones. Reprinted with permission from (68). Copyright 2020 American Chemical Society. (C) Cumulative release profile of FGF-18 from PLGA hydrogel, and (D) histological images demonstrating tissue regeneration in a murine calvarial defect model treated with FGF-18–loaded PLGA hydrogel. Reprinted with permission from (67). Copyright 2017 American Chemical Society.
이와 같이 합성 고분자 드레싱은 기능성과 적용성을 동시에 갖춘 유망한 구강 상처 치료 솔루션으로 부상하고 있다. 약물 전달, 항균 효과, 조직 재생 촉진 기능이 유기적으로 결합된 시스템은 기존의 단순 보호용 드레싱을 넘어 적극적인 치료 중심의 스마트 소재로 진화하고 있으며, 임상 적용 가능성 또한 점차 확대되고 있다.
4. 한계점과 향후 연구 방향
현재까지 개발된 합성 고분자 기반 구강 상처 드레싱은 물성 조절과 기능성 부여 측면에서 높은 가능성을 보여주고 있다. 그러나 실제 임상 적용에 있어서는 여전히 몇 가지 한계점과 기술적 과제가 존재한다. 첫째, 구강 내의 복잡한 해부학적 구조와 지속적인 기계적 자극, 삼킴 등의 요소는 드레싱의 고정성 및 유지력 확보에 어려움을 야기한다(39). 둘째, 일부 합성 고분자는 분해 산물의 장기 안전성, 삼킴 시 독성 여부, 점막 자극 가능성 등의 생체 반응성 측면에서 추가적인 평가가 필요하다(69).
또한, 약물 전달, 항균력, 조직재생 등의 다양한 기능을 동시에 수행하는 다기능성 드레싱의 경우, 구조적 복잡성 증가로 인해 제조 공정이 까다롭고 비용이 상승하는 문제가 있을 것이다. 상용화를 위해서는 임상 현장에서의 적용 용이성과 환자의 순응도를 높일 수 있는 설계가 중요하며, 이를 위한 포장성, 사용성, 저장 안정성 등의 요소도 함께 고려되어야 한다(70). 실제 사용 환경에서 드레싱의 탈락 빈도, 교체 주기, 환자의 불편감 등은 아직 충분히 연구되지 않은 영역이다.
향후 연구에서는 구강에 적합한 환경 적응성을 갖춘 소재 개발과 함께, 맞춤형 드레싱 시스템, 바이오 프린팅 기반 상처 재건 플랫폼, 그리고 임상 유효성 검증을 위한 대규모 연구가 필요하다. 또한, 단일 소재 중심의 연구에서 벗어나 복합재 기반의 융합형 드레싱 개발을 통해 구강 상처 치유의 새로운 해법을 제시할 수 있을 것이다.
결 론
합성 고분자 기반 드레싱은 구강 내 상처 치료에 있어, 습윤하고 역동적이며 미생물이 풍부한 환경이라는 고유한 도전 과제를 해결할 수 있는 유망하고 유연한 플랫폼으로 주목받고 있다. 이러한 드레싱은 정교한 소재 설계를 통해 물리적 보호뿐 아니라, 약물 전달, 항균 효과, 조직 재생 유도 등 능동적인 치료 기능을 동시에 수행할 수 있다. 스마트 고분자 시스템과 자극 반응형 제형, 임상 적용 기술의 발전이 지속됨에 따라, 합성 고분자는 차세대 구강 상처 관리의 핵심 소재로 자리매김할 것으로 기대된다. 본 리뷰는 주요 소재와 기능적 전략, 적용 사례들을 정리함으로써 향후 연구 방향을 제시하고, 보다 효과적이고 환자 친화적인 구강 상처 드레싱 개발에 기여하고자 한다.
본 리뷰에서 다룬 주요 합성 고분자(PVA, PEG, PLGA, PU, PCL 등)는 물리적 특성, 기능적 장점, 구강 내 적용 가능성에 따라 각각 고유한 장단점을 지니며, 그 요약은 본문 Table 1에 정리하였다. 이러한 재료들은 설계 유연성과 기능성 부여 측면에서 높은 가능성을 보이지만, 실제 임상 적용을 위해서는 독성 및 생체적합성 평가, 장기 안정성 확보, 규제 승인 요건 충족 등의 추가적 검증이 필수적이다, . 특히 향후 연구에서는 상용화를 위한 제조공정의 표준화, 임상 시험 기반의 과학적 근거 확보, 그리고 제품화 과정에서의 법적·윤리적 기준에 대한 종합적인 검토가 병행되어야 한다.
Acknowledgments
이 논문은 2023년도 강릉원주대학교 치과병원 협동임상연구비(CR2302) 지원에 의하여 수행되었음.
References
-
Fitzpatrick SG, Cohen DM, Clark AN. Ulcerated Lesions of the Oral Mucosa: Clinical and Histologic Review. Head Neck Pathol. 2019;13(1):91-102.
[https://doi.org/10.1007/s12105-018-0981-8]

-
Mortazavi H, Safi Y, Baharvand M, Rahmani S. Diagnostic Features of Common Oral Ulcerative Lesions: An Updated Decision Tree. Int J Dent. 2016;2016:7278925.
[https://doi.org/10.1155/2016/7278925]

-
Toma AI, Fuller JM, Willett NJ, Goudy SL. Oral wound healing models and emerging regenerative therapies. Transl Res. 2021;236:17-34.
[https://doi.org/10.1016/j.trsl.2021.06.003]

-
Marques Vieira B, Dias de Almeida Neto N, Everton Simoes L, Jorge Feres-Filho E, Ignez CG-EM, Xavier-Elsas P. Effects of oral wound on the neutrophil lineage in murine bone-marrow: Modulation mechanism hindered by chlorhexidine. Int Immunopharmacol. 2022;105:108544.
[https://doi.org/10.1016/j.intimp.2022.108544]

-
Qi W, Dong N, Wu L, Zhang X, Li H, Wu H, et al. Promoting oral mucosal wound healing using a DCS-RuB(2)A(2) hydrogel based on a photoreactive antibacterial and sustained release of BMSCs. Bioact Mater. 2023;23:53-68.
[https://doi.org/10.1016/j.bioactmat.2022.10.027]

-
Dragovic M, Pejovic M, Stepic J, Colic S, Dozic B, Dragovic S, et al. Comparison of four different suture materials in respect to oral wound healing, microbial colonization, tissue reaction and clinical features-randomized clinical study. Clin Oral Investig. 2020;24(4):1527-41.
[https://doi.org/10.1007/s00784-019-03034-4]

-
Chen Y, Gao B, Cai W, Lai J, Lai K, Wang Y. Oral mucosa: anti-inflammatory function, mechanisms, and applications. J Mater Chem B. 2025;13(13):4059-72.
[https://doi.org/10.1039/d4tb02845g]

-
Samiraninezhad N, Rezazadeh H, Rezazadeh H, Mardaninezhad R, Tabesh A, Rezazadeh F. Platelet-rich fibrin in the management of oral mucosal lesions: a scoping review. BMC Oral Health. 2024;24(1):1189.
[https://doi.org/10.1186/s12903-024-04981-5]

-
Hodge JG, Zamierowski DS, Robinson JL, Mellott AJ. Evaluating polymeric biomaterials to improve next generation wound dressing design. Biomater Res. 2022;26(1):50.
[https://doi.org/10.1186/s40824-022-00291-5]

-
Wei YZ, Zheng LN, Xie X, Yang X, Liao JF. Recent advances in stimuli responsive hydrogels for oral disease treatment. Mater Design. 2024;240.
[https://doi.org/10.1016/j.matdes.2024.112817]

-
Wang ZC, Han X, Xiao WW, Wang P, Wang JH, Zou D, et al. Mussel-inspired adhesive drug-loaded hydrogels for oral ulcers treatment. Acta Biomater. 2024;187:98-109.
[https://doi.org/10.1016/j.actbio.2024.08.038]

-
Huang Z, Wang M, Chai LJ, Chen H, Chen DY, Li YL, et al. Glucose-responsive, self-healing, wet adhesive and multi-biofunctional hydrogels for diabetic wound healing. Mater Today Bio. 2024;27.
[https://doi.org/10.1016/j.mtbio.2024.101159]

-
Faran Ali SM, Tanwir F. Oral microbial habitat a dynamic entity. J Oral Biol Craniofac Res. 2012;2(3):181-7.
[https://doi.org/10.1016/j.jobcr.2012.07.001]

- Tian S, Ding T, Li H. Oral microbiome in human health and diseases. mLife. 2024;3(3):367-83.
-
Cai EY, Qi XL, Shi YZ, Ge XX, Xiang YJ, Xu HB, et al. Immunomodulatory melanin@Pt nanoparticle-reinforced adhesive hydrogels for healing diabetic oral ulcers. Chem Eng J. 2024;488.
[https://doi.org/10.1016/j.cej.2024.150372]

-
Wang Y, Pan Z, Cui J, Zhang X, Li D, Sun H, et al. Adhesive hydrogel releases protocatechualdehyde-Fe(3+) complex to promote three healing stages for accelerated therapy of oral ulcers. Acta Biomater. 2024;178:68-82.
[https://doi.org/10.1016/j.actbio.2024.02.047]

-
Fan ML, Yang JJ, Zhen L, Zhu JY, Liang KN, Li JY. A mussel-inspired wet-adhesive prolonged-acting antibacterial hydrogels for the treatment of periodontitis. Chem Eng J. 2025;509.
[https://doi.org/10.1016/j.cej.2025.161262]

-
Li G, Pu Z, Guo S, Liu Z, Deng M, Liu N, et al. Durable and biocompatible low adhesion wound dressing material based on interfacial behaviors for wound management. Colloids Surf B Biointerfaces. 2025;247:114413.
[https://doi.org/10.1016/j.colsurfb.2024.114413]

-
Chen HG, Zhao ZF, Zhang R, Zhang G, Liang XY, Xu C, et al. Adaptable Hydrogel with Strong Adhesion of Wet Tissue for Long-Term Protection of Periodontitis Wound. Adv Mater. 2025;37(1).
[https://doi.org/10.1002/adma.202413373]

-
Vasilev O, Hayles A, Campbell D, Jaarsma R, Johnson L, Vasilev K. Nanoscale antibacterial coatings incorporating silver nanoparticles derived by plasma techniques - A state-of-the-art perspective. Mater Today Chem. 2024;41.
[https://doi.org/10.1016/j.mtchem.2024.102341]

-
Rojo L, Garcia-Fernandez L, Aguilar MR, Vazquez-Lasa B. Antimicrobial polymeric biomaterials based on synthetic, nanotechnology, and biotechnological approaches. Curr Opin Biotechnol. 2022;76:102752.
[https://doi.org/10.1016/j.copbio.2022.102752]

-
Xia XY, Jia X, Yu ZQ, Zhang GY, Su ZH. Responsive antibacterial surface based on looped poly (methacrylic acid). Appl Surf Sci. 2024;665.
[https://doi.org/10.1016/j.apsusc.2024.160361]

-
Wang X, Song L, Zhao J, Zhou R, Luan S, Huang Y, et al. Bacterial adaptability of enzyme and pH dual-responsive surface for infection resistance. J Mater Chem B. 2018;6(46):7710-8.
[https://doi.org/10.1039/c8tb01950a]

-
Wu J, Pan Z, Zhao ZY, Wang MH, Dong L, Gao HL, et al. Anti-Swelling, Robust, and Adhesive Extracellular Matrix-Mimicking Hydrogel Used as Intraoral Dressing. Adv Mater. 2022;34(20).
[https://doi.org/10.1002/adma.202200115]

-
Izumi K, Yortchan W, Aizawa Y, Kobayashi R, Hoshikawa E, Ling Y, et al. Recent trends and perspectives in reconstruction and regeneration of intra/extra-oral wounds using tissue-engineered oral mucosa equivalents. Jpn Dent Sci Rev. 2023;59:365-74.
[https://doi.org/10.1016/j.jdsr.2023.10.002]

-
Tirupathi S, Afnan L. Effectiveness of Reso-Pac® in Post-Operative Intraoral Wound Healing Parameters Related to Third Molar Extraction. Journal of Maxillofacial and Oral Surgery. 2025.
[https://doi.org/10.1007/s12663-025-02455-x]

-
Gao X, Wen M, Liu Y, Hou T, An M. Mechanical performance and cyocompatibility of PU/PLCL nanofibrous electrospun scaffolds for skin regeneration. Engineered Regeneration. 2022;3(1):53-8.
[https://doi.org/10.1016/j.engreg.2022.01.002]

-
Çakmen AB, Noma SAA, Gürses C, Köytepe S, Ates B, Yilmaz I. The preparation of trimethylolpropane ethoxylate-170-based antibacterial wound dressing materials containing allantoin via electrospinning method. Polym Bull. 2024;81(18):16801-26.
[https://doi.org/10.1007/s00289-024-05493-6]

-
Baker SR, Banerjee S, Bonin K, Guthold M. Determining the mechanical properties of electrospun poly-epsilon-caprolactone (PCL) nanofibers using AFM and a novel fiber anchoring technique. Mater Sci Eng C Mater Biol Appl. 2016;59:203-12.
[https://doi.org/10.1016/j.msec.2015.09.102]

-
Silva MdS, Neto NL, da Costa SA, da Costa SM, Oliveira TM, Oliveira RCd, et al. Biophysical and biological characterization of intraoral multilayer membranes as potential carriers: A new drug delivery system for dentistry. Mat Sci Eng C-Mater. 2017;71:498-503.
[https://doi.org/10.1016/j.msec.2016.10.032]

-
Tao YH, Tan X, Zhang TZ. Enhancing biocompatibility and degradation control of biodegradable polymers through amino acid grafting: A study on 4arm-PLGA-Amino acid copolymers. Appl Mater Today. 2024;41.
[https://doi.org/10.1016/j.apmt.2024.102497]

-
Maeda T, Kitagawa M, Hotta A. Degradation of thermoresponsive laponite/PEG-b-PLGA nanocomposite hydrogels controlled by blending PEG-b-PLGA diblock copolymers with different PLGA molecular weights. Polym Degrad Stabil. 2021;187.
[https://doi.org/10.1016/j.polymdegradstab.2021.109535]

-
Zhou C, Sheng CJ, Chen JJ, Liang YH, Liu QP, Li P, et al. Gradual hydrogel degradation for programable repairing full-thickness skin defect wound. Chem Eng J. 2022;450.
[https://doi.org/10.1016/j.cej.2022.138200]

-
Moradifar F, Sepahdoost N, Tavakoli P, Mirzapoor A. Multi-functional dressings for recovery and screenable treatment of wounds: A review. Heliyon. 2025;11(1):e41465.
[https://doi.org/10.1016/j.heliyon.2024.e41465]

-
Lu C, Sun Q, Li Z, Wei Y, Yu J, Li S, et al. Injectable glycyrrhizinate-pectin hydrogel wound dressing based on natural ingredients. Carbohydrate Polymers. 2025;359:123562.
[https://doi.org/10.1016/j.carbpol.2025.123562]

-
Hu T, Wu GP, Bu HT, Zhang HY, Li WX, Song K, et al. An injectable, adhesive, and self-healable composite hydrogel wound dressing with excellent antibacterial activity. Chem Eng J. 2022;450.
[https://doi.org/10.1016/j.cej.2022.138201]

-
Ullah A, Jang M, Khan H, Choi HJ, An S, Kim D, et al. Microneedle array with a pH-responsive polymer coating and its application in smart drug delivery for wound healing. Sensor Actuat B-Chem. 2021;345.
[https://doi.org/10.1016/j.snb.2021.130441]

-
Rad I, Esmaeili E, Jahromi BB. Application of thermo-responsive polymers as smart biomaterials in wound dressing. Polym Bull. 2024;81(13):11399-420.
[https://doi.org/10.1007/s00289-024-05276-z]

- Ding Y, Zhu Z, Zhang X, Wang J. Novel Functional Dressing Materials for Intraoral Wound Care. Adv Healthc Mater. 2024;13(23):e2400912.
-
DeMerlis CC, Schoneker DR. Review of the oral toxicity of polyvinyl alcohol (PVA). Food Chem Toxicol. 2003;41(3):319-26.
[https://doi.org/10.1016/s0278-6915(02)00258-2]

-
Kamoun EA, Chen X, Mohy Eldin MS, Kenawy E-RS. Crosslinked poly(vinyl alcohol) hydrogels for wound dressing applications: A review of remarkably blended polymers. Arabian Journal of Chemistry. 2015;8(1):1-14.
[https://doi.org/10.1016/j.arabjc.2014.07.005]

-
Song S, Liu Z, Abubaker MA, Ding L, Zhang J, Yang SR, et al. Antibacterial polyvinyl alcohol/bacterial cellulose/nano-silver hydrogels that effectively promote wound healing. Mat Sci Eng C-Mater. 2021;126.
[https://doi.org/10.1016/j.msec.2021.112171]

-
Huang CY, Hu KH, Wei ZH. Comparison of cell behavior on pva/pva-gelatin electrospun nanofibers with random and aligned configuration. Sci Rep. 2016;6:37960.
[https://doi.org/10.1038/srep37960]

-
Wang Z, Ye Q, Yu S, Akhavan B. Poly Ethylene Glycol (PEG)-Based Hydrogels for Drug Delivery in Cancer Therapy: A Comprehensive Review. Adv Healthc Mater. 2023;12(18):e2300105.
[https://doi.org/10.1002/adhm.202370102]

-
Tirelli N, Lutolf MP, Napoli A, Hubbell JA. Poly (ethylene glycol) block copolymers. J Biotechnol. 2002;90(1):3-15.
[https://doi.org/10.1016/s1389-0352(01)00057-5]

-
Ibrahim M, Ramadan E, Elsadek NE, Emam SE, Shimizu T, Ando H, et al. Polyethylene glycol (PEG): The nature, immunogenicity, and role in the hypersensitivity of PEGylated products. J Control Release. 2022;351:215-30.
[https://doi.org/10.1016/j.jconrel.2022.09.031]

-
Marquina S, Ozgul M, Robertson-Brown K, Kenney MC. A review on PLGA particles as a sustained drug-delivery system and its effect on the retina. Exp Eye Res. 2023;235.
[https://doi.org/10.1016/j.exer.2023.109626]

-
Hong MH, Choi HJ, Ko YM, Lee YK. Engineered microstructure granules for tailored drug release rate. Biotechnol Bioeng. 2015;112(9):1936-47.
[https://doi.org/10.1002/bit.25595]

-
Vo TN, Kasper FK, Mikos AG. Strategies for controlled delivery of growth factors and cells for bone regeneration. Adv Drug Deliv Rev. 2012;64(12):1292-309.
[https://doi.org/10.1016/j.addr.2012.01.016]

-
Lykins WR, Bernards DA, Schlesinger EB, Wisniewski K, Desai TA. Tuning polycaprolactone degradation for long acting implantables. Polymer. 2022;262.
[https://doi.org/10.1016/j.polymer.2022.125473]

-
Taekhyun K, Hyungjoon S, Min-Ho H. Physicochemical properties and biocompatibility of polypyrrole-coated polycaprolactone nanofibers for guided tissue regeneration. Korean Journal of Dental Materials. 2024;51(1):29-42.
[https://doi.org/10.14815/kjdm.2024.51.1.29]

-
Sharif F, Roman S, Asif A, Gigliobianco G, Ghafoor S, Tariq M, et al. Developing a synthetic composite membrane for cleft palate repair. J Tissue Eng Regen Med. 2019;13(7):1178-89.
[https://doi.org/10.1002/term.2867]

-
Jia B, Zhang B, Li J, Qin J, Huang Y, Huang M, et al. Emerging polymeric materials for treatment of oral diseases: design strategy towards a unique oral environment. Chem Soc Rev. 2024;53(7):3273-301.
[https://doi.org/10.1039/d3cs01039b]

-
Zhang J, Li Y, Sheng G. Nanodiamond-Reinforced Polyurethane Micro/Nanofiber Membrane for UV Protection in Multifunctional Textiles. ACS Applied Nano Materials. 2024;7(11):12323-33.
[https://doi.org/10.1021/acsanm.4c00078]

-
Ewedah TM, Abdalla A, Hagag RS, Elhabal SF, Teaima MH, El-Nabarawi MA, et al. Enhancing cellular affinity for skin disorders: Electrospun polyurethane/collagen nanofiber mats coated with phytoceramides. Int J Pharm. 2024;663:124541.
[https://doi.org/10.1016/j.ijpharm.2024.124541]

-
Carbonell JM, Martin IS, Santos A, Pujol A, Sanz-Moliner JD, Nart J. High-density polytetrafluoroethylene membranes in guided bone and tissue regeneration procedures: a literature review. Int J Oral Maxillofac Surg. 2014;43(1):75-84.
[https://doi.org/10.1016/j.ijom.2013.05.017]

-
Barber HD, Lignelli J, Smith BM, Bartee BK. Using a dense PTFE membrane without primary closure to achieve bone and tissue regeneration. J Oral Maxillofac Surg. 2007;65(4):748-52.
[https://doi.org/10.1016/j.joms.2006.10.042]

-
Swift T, Swanson L, Geoghegan M, Rimmer S. The pH-responsive behaviour of poly(acrylic acid) in aqueous solution is dependent on molar mass. Soft Matter. 2016;12(9):2542-9.
[https://doi.org/10.1039/c5sm02693h]

-
Sridhar SP, Soman AK, Sankaran TS, Chandran S, Joseph B. Temperature Responsive Poly (N-isopropylacrylamide-block-styrene) Block Copolymer Coatings with Tunable Hydrophilicity. Surf Interfaces. 2020;21.
[https://doi.org/10.1016/j.surfin.2020.100800]

-
Barroso-Solares S, Pinto J, Salvo-Comino C, Cuadra-Rodr guez D, Garc a-Cabez n C, í í ó Rodríguez-Pérez MA, et al. Tuning the electrochemical response of PCL-PEDOT: PSS fibers-based sensors by gas dissolution foaming. Appl Surf Sci. 2023;638.
[https://doi.org/10.1016/j.apsusc.2023.158062]

-
Haktaniyan M, Bradley M. Polymers showing intrinsic antimicrobial activity. Chemical Society Reviews. 2022;51(20):8584-611.
[https://doi.org/10.1039/d2cs00558a]

-
Sutthiwanjampa C, Hong S, Kim WJ, Kang SH, Park H. Hydrophilic Modification Strategies to Enhance the Surface Biocompatibility of Poly(dimethylsiloxane)- Based Biomaterials for Medical Applications. Adv Mater Interfaces. 2023;10(12).
[https://doi.org/10.1002/admi.202202333]

-
Chen S, Liu B, Carlson MA, Gombart AF, Reilly DA, Xie J. Recent advances in electrospun nanofibers for wound healing. Nanomedicine (Lond). 2017;12(11):1335-52.
[https://doi.org/10.2217/nnm-2017-0017]

-
Zhuang Y, Wu D, Zhou L, Liu B, Zhao X, Yang J, et al. Electrospun Biomimetic Periosteum Promotes Diabetic Bone Defect Regeneration through Regulating Macrophage Polarization and Sequential Drug Release. ACS Biomaterials Science & Engineering. 2025;11(3):1690-704.
[https://doi.org/10.1021/acsbiomaterials.4c02095]

-
Kang S, Jang EJ, Jo HM, Kang SS, Lee MS, Yun SY, et al. Effects of a Topically Applied Oral Wound Dressing Film on Intra-oral Wound Healing in Rabbits. In Vivo. 2022;36(4):1745-52.
[https://doi.org/10.21873/invivo.12887]

- Kennedy TJ, Hall JE. A drug-free oral hydrogel wound dressing for pain management in immediate denture patients. Gen Dent. 2009;57(4):420-7.
-
Sivashanmugam A, Charoenlarp P, Deepthi S, Rajendran A, Nair SV, Iseki S, et al. Injectable Shear-Thinning CaSO4/FGF-18-Incorporated Chitin–PLGA Hydrogel Enhances Bone Regeneration in Mice Cranial Bone Defect Model. ACS Applied Materials & Interfaces. 2017;9(49):42639-52.
[https://doi.org/10.1021/acsami.7b15845]

-
Haidari H, Kopecki Z, Bright R, Cowin AJ, Garg S, Goswami N, et al. Ultrasmall AgNP-Impregnated Biocompatible Hydrogel with Highly Effective Biofilm Elimination Properties. ACS Appl Mater Interfaces. 2020;12(37):41011-25.
[https://doi.org/10.1021/acsami.0c09414]

-
Pappalardo D, Mathisen T, Finne-Wistrand A. Biocompatibility of Resorbable Polymers: A Historical Perspective and Framework for the Future. Biomacromolecules. 2019;20(4):1465-77.
[https://doi.org/10.1021/acs.biomac.9b00159]

-
Packaging for terminally sterilized medical devices : Part 1. Requirements for materials, sterile barrier systems and packaging systems : ISO 11607-1:2019. Geneva, Switzerland: International Organization for Standardization; 2019.
[https://doi.org/10.2345/9781570207211.ch1]


